题目内容
【题目】纯净的CaCO3粉末放入A试管中充分加热,按如图所示的顺序进行相关实验,回答问题。
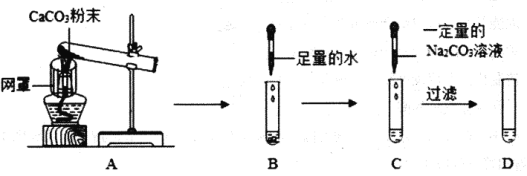
(1)写出装置A中的一种玻璃仪器___________________。
(2) A试管内发生的反应,用于工业制备___________________、生石灰;
(3) B试管发生的反应,用化学方程式表示为___________________。
(4) C试管内能观察到的实验现象是___________________。
(5)要验证D试管溶液中可能含有Ca2+或CO32-,选用下列试剂中的___________________。
A BaCl2溶液
B Na2CO3 溶液
C NaCl 溶液
D 酚酞溶液
【答案】试管或酒精灯 二氧化碳 CaO+H2O=Ca (OH) 2 产生白色沉淀 AB
【解析】
(1)由图可知装置中有酒精灯和试管属于玻璃仪器,故填:酒精灯或试管。
(2)碳酸钙高温生成氧化钙和二氧化碳,A试管内发生的反应,用于工业制备二氧化碳和生石灰,故填:二氧化碳。
(3)氧化钙和水反应生成氢氧化钙,化学方程式为CaO+H2O=Ca (OH) 2,故填:CaO+H2O=Ca (OH) 2。
(4)氢氧化钙和碳酸钠反应生成碳酸钙白色沉淀和氢氧化钠,故填:产生白色沉淀。
(5)要验证D试管溶液中可能含有Ca2+或CO32-:
A、 BaCl2溶液中钡离子和碳酸根离子生成碳酸钡沉淀,根据是否产生沉淀可判定是否有碳酸根离子符合题意。
B 、Na2CO3 溶液中碳酸根离子和钙离子生成碳酸钙沉淀,根据是否产生沉淀可判定是否有钙离子符合题意。
C、NaCl 溶液和钙离子碳酸根离子,都不反应,无现象,无法鉴别,不符合题意。
D、C试管加入碳酸钠,氢氧化钙可能没有完全反应,加入酚酞溶液,溶液变红无法判断是否含有碳酸根离子,不符合题意。
故选:AB。