题目内容
在一密闭容器中,有甲、乙、丙、丁四种物质,在一定条件下存在某个反应,测得反应前后各物质的质量如下表:
对该反应,下列描述中正确的是( )
| 物质 | 甲 | 乙 | 丙 | 丁 |
| 反应前质量/g | 20 | m | 8 | 6 |
| 反应后质量/g | 4 | 待测 | 28 | 2 |
| A、反应中甲和丙的质量比为2:3 |
| B、乙一定是该反应的催化剂 |
| C、该反应可能是铜与氧气的反应 |
| D、该反应是分解反应 |
考点:质量守恒定律及其应用,催化剂的特点与催化作用,反应类型的判定
专题:化学用语和质量守恒定律
分析:反应后甲的质量减少16g,是反应物;
反应后丙的质量增加20g,是生成物;
反应后丁的质量减少4g,是反应物;
根据质量守恒定律可知,反应的乙的质量为:16g+4g-20g=0,即乙物质没有参加反应.
反应后丙的质量增加20g,是生成物;
反应后丁的质量减少4g,是反应物;
根据质量守恒定律可知,反应的乙的质量为:16g+4g-20g=0,即乙物质没有参加反应.
解答:解:A、反应中甲和丙的质量比为:16g:20g=4:5,该选项说法不正确;
B、乙可能是该反应的催化剂,也可能既不是催化剂,也不是反应物和生成物,该选项说法不正确;
C、铜和氧气反应的化学方程式及其反应物、生成物之间的质量比为:2Cu+O2
2CuO,
128 32 160
128:32:160=16:4:20,该选项说法正确;
D、该反应中,反应物是两种,生成物是一种,属于化合反应,该选项说法不正确.
故选:C.
B、乙可能是该反应的催化剂,也可能既不是催化剂,也不是反应物和生成物,该选项说法不正确;
C、铜和氧气反应的化学方程式及其反应物、生成物之间的质量比为:2Cu+O2
| ||
128 32 160
128:32:160=16:4:20,该选项说法正确;
D、该反应中,反应物是两种,生成物是一种,属于化合反应,该选项说法不正确.
故选:C.
点评:化学反应遵循质量守恒定律,即化学反应前后,元素的种类不变,原子的种类、总个数不变,这是书写化学方程式、进行相关方面计算的基础.

练习册系列答案
相关题目
要使硝酸钾的溶解度增大,可采用的措施是( )
| A、加硝酸钾 | B、升高温度 |
| C、快速搅拌 | D、蒸发水分 |
在2011年12月闭幕的南非德班世界气候大会主题是节能减排,低碳生活.下列做法不属于“低碳”的是( )
| A、将煤制成蜂窝煤 |
| B、电子贺卡代替纸质贺卡 |
| C、使用太阳能交通信号灯 |
| D、汽车安装尾气净化装置 |
下列关于合金的叙述中正确的是( )
| A、金属形成合金之后失去金属光泽 |
| B、只有金属和金属之间才能形成合金 |
| C、铁合金比纯铁的应用范围更广泛 |
| D、合金不能够传热、导电 |
以下叙述中不正确的是( )
| A、锌比铁活泼,但把锌镀在铁表面能防止铁生锈 |
| B、钛和钛合金是制造飞机和轮船的理想材料 |
| C、铝是地壳中含量最多的金属元素 |
| D、铜的化学性质不活泼,因此是制炊具的良好材料 |
下列化学现象描述不正确的是( )
| A、把盛有硫的燃烧匙伸进充满氧气的集气瓶中,硫立即燃烧 |
| B、硫在空气里燃烧发出微弱的淡蓝色火焰,生成一种有刺激性气味的气体 |
| C、硫在氧气里燃烧发出明亮的蓝紫色火焰,生成一种有刺激性气味的气体 |
| D、铝箔在氧气里剧烈燃烧,发出耀眼的白光,生成一种白色固体 |
不能用于加热的玻璃仪器是( )
| A、烧杯 | B、量筒 | C、蒸发皿 | D、试管 |
下列物质中,既有游离态的氧,又有化合态的氧是( )
| A、氯酸钾 | B、空气 |
| C、液氧 | D、二氧化锰 |
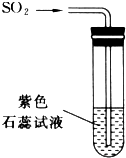 已知常温下二氧化硫是无色气体,它能与水反应生成亚硫酸:
已知常温下二氧化硫是无色气体,它能与水反应生成亚硫酸: