题目内容
【题目】神舟十一号飞船与天宫二号交会对接。太空中可使用过氧化钠作为氧气再生剂,Na2O2是一种淡黄色固体,常温下能与水和二氧化碳发生化学反应。
(1)在常温下,过氧化钠Na2O2能与航天员呼出的CO2反应生成碳酸钠和氧气,发生反应的化学方程式为2Na2O2+2CO2=2Na2CO3+O2,可是有同学认为该反应还可能生成碳酸氢钠(化学式为NaHCO3)和氧气,你认为他的说法是否正确,请简述你的看法和理由_______。
(2)常温下,过氧化钠也能与水发生反应,可以产生氧气,同时生成氢氧化钠,请写出该反应的化学方程式为______;
(3)若中国空间站内两位航天员在一定时间内所排出CO2的质量为88g,完全吸收这些排出物,则需要消耗过氧化钠的质量为____g,同时产生通常状况下氧气的体积为____L(通常状况下的氧气密度为1.43g/L,计算结果确到0.1)。
【答案】不正确;因为反应物中不含H元素 ![]() 156 22.4
156 22.4
【解析】
(1)不正确,根据质量守恒定律,化学反应前后,原子的种类和数目不变,反应物中不含氢元素,不可能生成碳酸氢钠;
(2)常温下,过氧化钠能与水发生反应,产生氧气,同时生成氢氧化钠,该反应的化学方程式为:![]() ;
;
(3)设需要消耗过氧化钠的质量为x,生成氧气的质量为y。
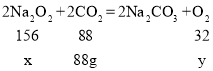
![]() x=156g
x=156g
![]() y=32g
y=32g
产生氧气的体积为:32g÷1.43g/L≈22.4L。

【题目】化学小组同学在课外读物中看到:“通常CO2可作灭火剂,但有些物质(如Na)着火,不能用CO2熄灭” 。他们决定探究CO2与Na反应的产物。
(提出猜想)CO2与Na反应可能生成4种物质:C、CO、Na2O、Na2CO3。
(查阅资料)
①Na是非常活泼的金属,常温下与O2、H2O等物质反应。
②碱性的Na2CO3溶液与中性的CaCl2溶液发生复分解反应。
③Na2O是白色固体,与H2O反应生成NaOH。
④向氯化钯(PdCl2)溶液中通入CO,产生黑色沉淀。
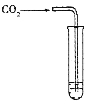
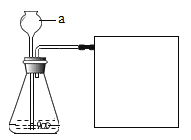
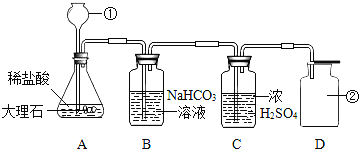
(实验过程)同学们在老师的指导下设计了如下图所示装置(部分夹持仪器已略去)
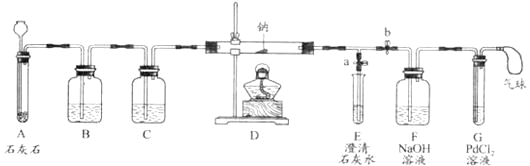
(1)实验记录
序号 | 实验操作 | 主要实验现象 | 实验结论和解释 |
① | 打开a,关闭b,由长颈漏斗注入稀盐酸 | A中产生大量气泡 | E中反应的化学方程式为_____________ |
② | 当E中出现浑浊时,打开b,关闭a,点燃酒精灯 | D中Na剧烈燃烧,产生白烟内壁附着黑色、白色固体 | 反应产物一定有_______和_______ |
③ | 取D中白色固体于试管中,加水溶解,再加入石灰水 | 产生白色沉淀 | 反应产物还有________ |
(2)实验反思
①实验记录②中,E中出现浑浊,再点燃酒精灯的目的是___________。
②若无装置C,对实验有影响的物质是__________。
③检验第4种物质是否存在的实验方案:取D中白色固体于试管中,
。