题目内容
【题目】在化学学习中,了解知识的发展历程,可以促进我们正确理解科学本质。
(1)火药起源于唐朝,制作烟花的火药中加入镁粉,是为了引燃后能看到_____。
(2)十八世纪,化学家发现某些金属与酸反应能生成一种气体,该气体被喻为“会制造水的物质”,写出该气体燃烧制造水的化学方程式:_____。
(3)俄国化学家贝开托夫于1865年发表了金属活动性顺序。某同学将铝片放入氯化铜溶液中,发现有红色固体和无色气体生成。
①写出生成红色固体的化学方程式:_____。
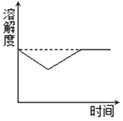
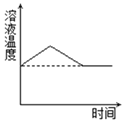
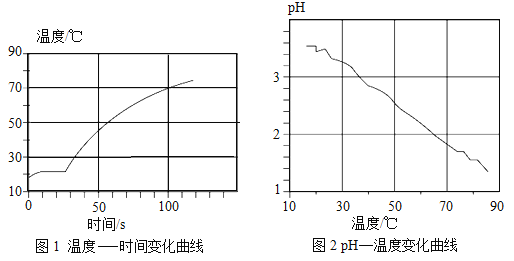
②利用温度传感器和pH传感器监测实验过程中的相关数据(如图所示),说明该过程_____(填“放热”或“吸热”),溶液的酸性_____(填“增强”或“减弱”);推测铝与溶液中的_____(填离子符号)反应生成无色气体_____(填物质名称)。
【答案】耀眼的白光 2H2+O2![]() 2H2O 2Al+3CuCl2═2AlCl3+3Cu 放热 增强 H+ 氢气
2H2O 2Al+3CuCl2═2AlCl3+3Cu 放热 增强 H+ 氢气
【解析】
解:(1)由于镁燃烧能发出耀眼的白光,所以制作烟花的火药中加入镁粉,是为了引燃后能看到耀眼的白光;
(2)氢气和氧气在点燃的条件下生成水,化学方程式为:2H2+O2![]() 2H2O;
2H2O;
(3)①由于铝的金属活动性大于铜,能将铜从其溶液中置换出来,反应的化学方程式:2Al+3CuCl2═2AlCl3+3Cu;
②由温度传感器和pH传感器监测实验过程中的相关数据可知,溶液的温度升高,说明该过程放热,溶液的pH减小,说明酸性增强;据此可推测铝与溶液中的H+反应生成无色气体氢气。

练习册系列答案
相关题目