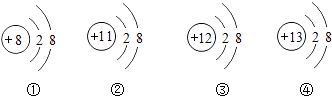
��Ŀ����
����Ŀ��ijˮ�೧�����ң�Ϊ�˲ⶨij��ɽʯ��ʯ��̼��Ƶ�����������ȡʯ��ʯ��Ʒ������ϡ�������ձ��з�Ӧ������ʯ��ʯ��Ʒ�����ʲ���ϡ���ᷴӦҲ������ˮ�����й�ʵ���������±���
��Ӧǰ | ��Ӧ�� | ||
ʵ | �ձ���ϡ���� | ʯ��ʯ��Ʒ | �ձ������л� |
150g | 12g | 157.6g | |
��1�����������غ㶨�ɿ�֪����Ӧ�����ɶ�����̼������Ϊg��
��2�����ʯ��ʯ��̼��Ƶ�����������
���𰸡�
��1��4.4
��2��
�⣺���ʯ��ʯ��Ʒ��̼��Ƶ�����Ϊx��
CaCO3+2HCl�TCaCl2+H2O+CO2��
100 44
x 4.4g
![]() ��x=10g
��x=10g
��ʯ��ʯ��̼��Ƶ���������Ϊ�� ![]() ��100%��83.3%
��100%��83.3%
�𣺸�ʯ��ʯ��̼��Ƶ���������Ϊ83.3%��
���������⣺��1�����������غ㶨�ɣ�������̼������Ϊ��150g+12g��157.6g=4.4g��
��1�����������غ㶨�ɿ�֪����Ӧ��ȷ�Ӧǰ���ٵ����������ɶ�����̼����������2�����ݻ�ѧ����ʽ�ɶ�����̼���������Լ����ʯ��ʯ��̼��Ƶ����������������ʯ��ʯ��̼��Ƶ�����������

��ϰ��ϵ�д�
 ��ѧ�����ϵ�д�
��ѧ�����ϵ�д� �·Ƿ��̸����100��ϵ�д�
�·Ƿ��̸����100��ϵ�д�
�����Ŀ