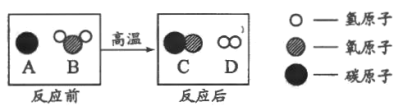
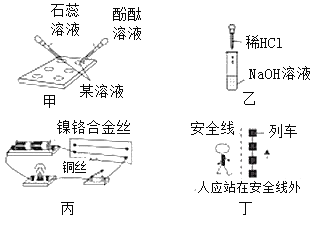
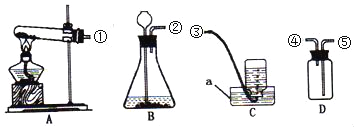
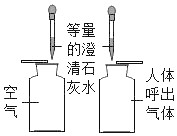
题目内容
【题目】甲、乙两种不含结品水的固体物质的溶解度曲线如图:
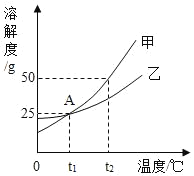
(1)A点的含义是_____。
(2)t2℃,将25g甲物质放入60g水中,充分溶解后,所得溶液是_____(填“饱和”或“不饱和”)溶液。
(3)t2℃,若从甲和乙两种物质的饱和溶液中析出等质量的固体,须蒸发掉较多水(温度不变)的是_____(填“甲”或“乙”)物质的饱和溶液。
(4)根据图中的溶解度曲线,下列说法正确的是_____。
A 温度由t2℃降到t1℃,含甲的溶液溶质质量分数一定减小
B t2℃时,可以配制溶质的质量分数为25%的甲溶液
C t2℃时,甲和乙各30g分别加入100g水中,充分溶解后同时等速降温,则乙溶液先达到饱和
D 甲中混有少量乙,可用蒸发结晶法提纯甲
【答案】在t1℃时,甲、乙的溶解度相等 不饱和 乙 BC
【解析】
根据题目信息和溶解度曲线可知:甲、乙两种固体物质的溶解度,都是随温度升高而增大,而甲的溶解度随温度的升高变化比乙大。
(1)A点的含义是:在t1℃时,甲、乙的溶解度相等;故填:在t1℃时,甲、乙的溶解度相等
(2)t2℃,将25g甲物质放入60g水中,充分溶解后,所得溶液是不饱和溶液,因为该温度下,甲的溶解度是30g;故填:不饱和
(3)t2℃,若从甲和乙两种物质的饱和溶液中析出等质量的固体,须蒸发掉较多水(温度不变)的是乙物质的饱和溶液,因为该温度下,甲的溶解度大于乙的溶解度;故填:乙
(4)根据图中的溶解度曲线,说法正确的是:t2℃时,可以配制溶质的质量分数为25%的甲溶液正确,因为该温度下甲饱和溶液的质量分数是33.3%;t2℃时,甲和乙各30g分别加入100g水中,充分溶解后同时等速降温,则乙溶液先达到饱和;故填:BC

【题目】为测定某铜锌合金中锌的含量,取50g样品进行实验,将l00g稀盐酸分五次加入该样品中(杂质不溶于水也不参与反应,反应原理为:Zn+2HCl=ZnCl2+H2↑),充分反应后测得生成气体的总质量如表所示:
加入稀盐酸的质量/g | 20 | 20 | 20 | 20 | 20 |
生成气体的总质量/g | 0.05 | 0.10 | m | 0.20 | 0.20 |
试求:(1)m的数值为___________。
(2)该铜锌合金中锌的质量分数是___________?(写出计算过程)