题目内容
【题目】如图中A、B、C、D、E是四种粒子的结构示意图,请回答下列问题:
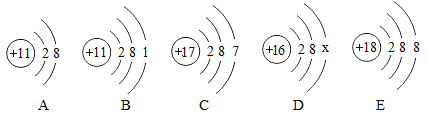
(1)图中A、B、C、D、E共包含_______种元素的粒子;
(2)A、B两种微粒的化学性质是_________(填“相似”、“不同”或“相同”);
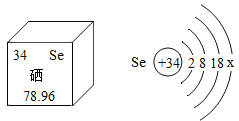
(3)若D为硫元素的原子结构示意图,则x=________,该粒子在化学变化中得电子而变成 ________ (用离子符号表示)。
(4)以上微粒中属于稳定结构的原子是___________(填字母)
(5)根据原子结构分析氯元素的最高正价是________.
【答案】4 不同 6 S2- E +7
【解析】
(1)由图中六种粒子的结构示意图可知,质子数是4种,属于4种元素的粒子;
(2)最外层电子数决定元素的化学性质,A、B两种微粒的最外层电子数不同,化学性质不同;
(3)若D为硫元素的原子结构示意图,则16=2+2+x,x=6,该粒子在化学变化中得到2个电子而变成带两个单位负电荷的硫离子,符号为:S2-;
(4)原子中,质子数=核外电子数,以上微粒中属于稳定结构的原子是E;
(5)一般情况下,元素的最高正价数与其原子的最外层电子数相等,故氯元素的最高正价是+7价。

练习册系列答案
 名题金卷系列答案
名题金卷系列答案
相关题目