题目内容
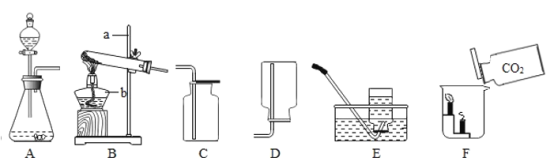
【题目】利用下图所示装置进行实验(装置气密性良好)。
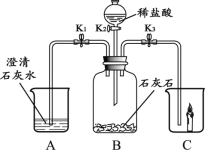
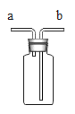
(1)打开K1、K2,注入一定量的稀盐酸后,关闭K2。观察到A中的现象是_____A中反应的化学方程式为____。B中反应的化学方程式为____。
(2)打开K3、关闭K1,观察到C中的蜡烛缓慢地熄灭。从灭火的原理回答蜡烛熄灭的原因是___
【答案】导管口处产生大量气泡,澄清的石灰水变浑浊 Ca(OH)2+CO2=H2O+CaCO3![]() CaCO3+2HCl=CaCl2+H2O+CO2↑ 产生不支持燃烧的二氧化碳,将燃烧的蜡烛与氧气隔绝
CaCO3+2HCl=CaCl2+H2O+CO2↑ 产生不支持燃烧的二氧化碳,将燃烧的蜡烛与氧气隔绝
【解析】
(1)打开K1、K2,注入一定量的稀盐酸后,B中石灰石遇到稀盐酸会产生气体,当关闭K2,B中会由于产生的气体而导致压强增大,伸向A的导管口处产生大量气泡,澄清的石灰水遇产生的气体会变浑浊,故填写:导管口处产生大量气泡,澄清的石灰水变浑浊;
氢氧化钙与二氧化碳反应,生成水和沉淀碳酸钙,故填写:Ca(OH)2+CO2=H2O+CaCO3![]() ;
;
稀盐酸与大理石反应生成氯化钙、水和二氧化碳,故填写:CaCO3+2HCl=CaCl2+H2O+CO2↑;
(2)打开K3、关闭K1,B中产生的二氧化碳会导向C中,由于二氧化碳不支持燃烧,不能燃烧,且密度比空气大,将燃烧的蜡烛与空气中氧气隔绝,蜡烛缓慢地熄灭,故填写:产生不支持燃烧的二氧化碳,将燃烧的蜡烛与氧气隔绝。

【题目】下表是NaCl和KNO3物质在不同温度下的部分溶解度数据(单位:g/100g水),请回答问题:
温度(℃) | 10 | 20 | 30 | 40 | 60 |
NaCl | 35.8 | 36.0 | 36.3 | 36.6 | 37.3 |
KNO3 | 20.9 | 31.6 | 45.8 | 63.9 | 110 |
(1)20℃时,NaCl的溶解度是_____g/100g水;
(2)以上两种物质溶解度变化受温度影响较小的是_____(选填“NaCl”或“KNO3”);
(3)20℃时,将20gNaCl固体加入50g水中,充分搅拌,形成的溶液质量为_____g;
(4)为了将混有少量NaCl杂质的KNO3的饱和溶液提纯,可通过_____方法获得较纯净的KNO3晶体;
(5)40℃时,将NaCl和KNO3的饱和溶液各100g降温到20℃,对剩余溶液描述正确的是_____。
A 溶质的质量分数:NaCl<KNO3
B 析出固体的质量:NaCl>KNO3
C NaCl和KNO3都是饱和溶液
D 溶剂的质量:NaCl>KNO3