题目内容
【题目】(12分)下图是实验室用碳酸钙与稀盐酸反应制取二氧化碳并验证其性质的的实验装置图,试根据题目要求回答下列问题:
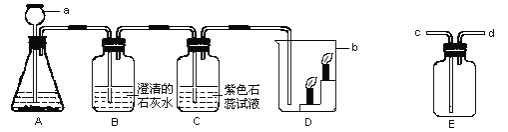
(1)仪器a的名称是 ;装置B中发生的化学方程式为 ;装置C中观察到的现象是 ;反应的化学方程式为: ;装置A中也可用于实验室制取 气体,制取该气体的化学方程式为 。
(2)装置D中观察到的现象是 ,说明二氧化碳的密度比空气大,它不能燃烧,也不能支持燃烧。由此可知,二氧化碳在生活中可用于 。
(3)实验室用装置E来收集二氧化碳时,二氧化碳应从 (填“c端”或“d端”)通入。
【答案】(1)长颈漏斗, Ca(OH)2+CO2==CaCO3↓+H2O ,紫色石蕊溶液变为红色,CO2+H2O==H2CO3, O2 ,
![]()
(2)低处的蜡烛先熄灭,高处的蜡烛后熄灭, 灭火。
(3)C
【解析】
试题分析:(1)该实验是实验室用碳酸钙与稀盐酸反应制取二氧化碳并验证其性质,故A装置的主要是生成二氧化碳,B装置是说明二氧化碳能与氢氧化钙反应,C装置是证明二氧化碳能与水反应生成碳酸:CO2+H2O==H2CO3,D装置是证明二氧化碳既不能燃烧也不支持燃烧。故B装置中二氧化碳与氢氧化钙反应生成的是氯化钙和水:Ca(OH)2+CO2==CaCO3↓+H2O;C装置中出现的现象是紫色石蕊溶液变为红色;A装置属固液在常温下反应的装置,故用于实验室用过氧化氢制取氧气或实验室制取氢气的反应装置;
(2)二氧化碳的密度比空气大,既不能燃烧也不能支持燃烧,故看到的 现象是:低处的蜡烛先熄灭,高处的蜡烛后熄灭,利用二氧化碳的该性质,二氧化碳能用于灭火;
(3)二氧化碳的密度比空气大,会先聚集在集气瓶的底部,故二氧化碳应从C端通入。

【题目】溶解度可以表示物质溶解性的大小。
① 下表是KNO3在不同温度下的溶解度。
温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 |
溶解度(g/100g水) | 13.3 | 31.6 | 63.9 | x | 169 | 246 |
Ⅰ.40℃时,硝酸钾的溶解度为 (8) g/100g水。
Ⅱ.40℃时将31 g KNO3固体放入50 g水中,所得溶液为 (9) 溶液(填“饱和”或“不饱和”),若降温到20℃能析出固体 (10) g。
Ⅲ.为测定x的值,取4份60℃的水各50 g,分别进行实验,并记录数据如下表:
实验编号 | 甲 | 乙 | 丙 | 丁 |
KNO3质量/g | 40 | 50 | 60 | 70 |
H2O质量/g | 50 | 50 | 50 | 50 |
溶液质量/g | 90 | 100 | 105 | 105 |
由实验可知 (11)
A.甲所得溶液中溶质质量分数为80%
B.乙恰好形成60℃时的饱和溶液
C.丙和丁所得溶液溶质质量分数相等
D.60℃时KNO3的溶解度为110g/100g水
② 气体的溶解度也有一定的变化规律。不同温度下,氧气的溶解度随压强变化如图所示,图中t1对应的温度为40℃,则t2对应的温度 (12)
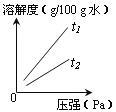
A.小于40℃ B.等于40℃ C.大于40℃ D.无法确定