题目内容
【题目】(6分)金属在日常生活中随处可见,研究金属的性质可以更好地利用金属。
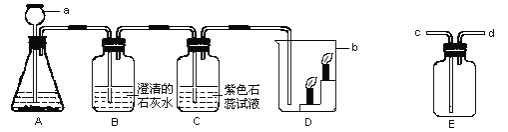
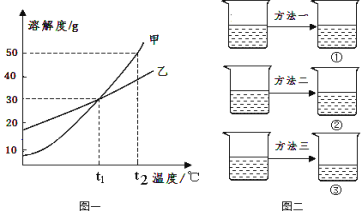
(1)下列生活用品中,主要利用金属导热性的是 (填序号)。

(2)“淬火”是金属热处理常用的方法。宝剑淬火过程中,铁在高温下和水蒸气发生反应生成四氧化三铁和另一种气体单质,该反应的化学方程式为 。
(3)将一定量铁粉加入到硫酸锌、硫酸铜的混合液中,充分反应后过滤。滤液中的溶质一定有 。
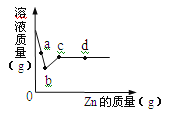
(4)取一定量镁、锌、铁三种金属,分别加入溶质质量分数相等的稀盐酸,充分反应后,生成氢气的质量相等。下列做法与此结果相符的是 (填序号)。
A.相同质量的三种金属与足量的稀盐酸反应
B.2.4 g镁、6.5 g锌、5.6 g铁与足量的稀盐酸反应
C.向足量的镁、锌、铁中加入稀盐酸的质量比为2︰3︰2
D.足量的三种金属与等量的稀盐酸反应
【答案】(1)② (2)3Fe +4H2O![]() Fe3O4 +4H2 (3)FeSO4、ZnSO4 (4)BD
Fe3O4 +4H2 (3)FeSO4、ZnSO4 (4)BD
【解析】
试题分析:铜制的火锅利用的是金属的导热性;宝剑淬火过程中,铁在高温下和水蒸气发生反
应生成四氧化三铁和另一种气体单质,该反应的化学方程式为3Fe +4H2O![]() Fe3O4 +4H2;将一定量铁粉加入到硫酸锌、硫酸铜的混合液中,充分反应后过滤。滤液中的溶质一定有FeSO4、ZnSO4;因为铁只能置换出铜而不能置换出锌;取一定量镁、锌、铁三种金属,分别加入溶质质量分数相等的稀盐酸,充分反应后,如果加入相同质量的三种金属与足量的稀盐酸反应,根据反应的情况产生的氢气的质量会是镁得到的最多,所以不会相等;当者的质量是2.4 g镁、6.5 g锌、5.6 g铁与足量的稀盐酸反应,产生的氢气的质量都是0.2克;所以符合题意;如果向足量的金属中倒入相同情况的酸后得到的氢气的质量也会相等,因为酸中含有氢元素的质量相同,所以被置换出的氢气的质量一定相等;所以C错误,而D正确。
Fe3O4 +4H2;将一定量铁粉加入到硫酸锌、硫酸铜的混合液中,充分反应后过滤。滤液中的溶质一定有FeSO4、ZnSO4;因为铁只能置换出铜而不能置换出锌;取一定量镁、锌、铁三种金属,分别加入溶质质量分数相等的稀盐酸,充分反应后,如果加入相同质量的三种金属与足量的稀盐酸反应,根据反应的情况产生的氢气的质量会是镁得到的最多,所以不会相等;当者的质量是2.4 g镁、6.5 g锌、5.6 g铁与足量的稀盐酸反应,产生的氢气的质量都是0.2克;所以符合题意;如果向足量的金属中倒入相同情况的酸后得到的氢气的质量也会相等,因为酸中含有氢元素的质量相同,所以被置换出的氢气的质量一定相等;所以C错误,而D正确。

 桃李文化快乐暑假武汉出版社系列答案
桃李文化快乐暑假武汉出版社系列答案 优秀生快乐假期每一天全新寒假作业本系列答案
优秀生快乐假期每一天全新寒假作业本系列答案