题目内容
【题目】室温下,向含有![]() 、
、![]() 、
、![]() 的混合溶液中加入一定质量的铁粉,充分反应后过滤,得到滤渣和滤液,将滤渣晾干后称量,质量为
的混合溶液中加入一定质量的铁粉,充分反应后过滤,得到滤渣和滤液,将滤渣晾干后称量,质量为![]() 。取少许滤渣,滴入稀盐酸,有气泡冒出,则下列判断中,正确的是( )
。取少许滤渣,滴入稀盐酸,有气泡冒出,则下列判断中,正确的是( )
A.滤液是无色溶液
B.滤液中一定含有![]() 、
、![]() 、
、![]()
C.加入铁粉的质量一定大于![]()
D.滤渣一定是![]() 、
、![]() 两种单质的混合物
两种单质的混合物
【答案】D
【解析】
由金属的活动性顺序可知,金属的活动性锌>铁>铜,室温下,向含有![]() 、
、![]() 、
、![]() 的混合溶液中加入一定质量的铁粉,铁不能与
的混合溶液中加入一定质量的铁粉,铁不能与![]() 、
、![]() 反应,能与
反应,能与![]() 反应生成
反应生成![]() 和铜,充分反应后过滤,得到滤渣和滤液,将滤渣晾干后称量,质量为ag。取少许滤渣,滴入稀盐酸,有气泡冒出,说明铁粉有剩余,滤液中不含有
和铜,充分反应后过滤,得到滤渣和滤液,将滤渣晾干后称量,质量为ag。取少许滤渣,滴入稀盐酸,有气泡冒出,说明铁粉有剩余,滤液中不含有![]() ,滤渣为铜和铁的混合物。
,滤渣为铜和铁的混合物。
A、由于溶液中含有![]() ,滤液是浅绿色的,A错误;
,滤液是浅绿色的,A错误;
B、由于铁有剩余,溶液中不含有氯化铜,滤液中一定不含有![]() ,B错误;
,B错误;
C、由于每56份质量的铁能置换出64份质量的铜,参加反应的铁的质量小于生成的铜的质量,C错误;
D、由上述分析可知,滤渣一定是Cu、Fe两种单质的混合物,D正确。故选D。

 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案【题目】某化学兴趣小组的同学按图示装置验证氢氧化钠的化学性质。
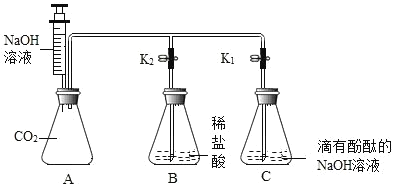
[实验步骤]
Ⅰ.关闭K1、K2,将注射器内的液体注入装置A中的锥形瓶内;
Ⅱ.打开K1,观察到装置C中部分红色溶液沿导管倒吸入装置A中,片刻后回流停止;
Ⅲ.打开K2,观察到装置B中溶液倒吸入装置A、C中,液面稳定后观察到装置A中溶液仍为红色,装置C中溶液变为无色。
同学们对相关问题分组展开如下探究:
探究环节 | 甲组的探究 | 乙组的探究 |
[提出问题] | 装置A中使酚酞变为红色的物质是什么? | 装置C中溶液为什么变成无色? |
[作出猜想] | 猜想一: Na2CO3; 猜想二: Na2CO3和NaOH | 猜想一:实验过程中酚酞变质了; 猜想二:溶液中的NaOH反应完了。 |
[实验验证] | ①小鹏取少量装置A中溶液于试管中,向其中滴加过量BaCl2溶液,若观察到_____,则证明猜想二成立; ②小丽认为用 | ①取少量装置C中溶液于试管中,向其中滴加NaOH溶液,溶液又变为红色,证明猜想一不成立; ②用pH试纸测定装置C 中溶液的酸|碱度,若pH_____, 则证明猜想二成立。 |
[反思交流]
(1)甲、乙两组同学的实验证明了NaOH能与稀盐酸、CO2发生反应,装置A中溶液里一定还存在NaCl;
(2)[实验步骤] II 中的现象_____(选填“能”或“不能”)证明NaOH与CO2发生了反应。
[拓展迁移]
综上所述,对于无明显现象的化学反应,要证明反应确实发生,可通过检验_____的方法实现。