题目内容
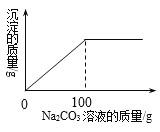
【题目】某盐矿井采出的食盐(俗称井盐)中含有CaCl2,为测定CaCl2的含量;准确称量上述井盐22.8g,向其中加入87.2克水使其完全溶解,然后向其中加入10.6%的Na2CO3溶液,生成沉淀的质量与加入Na2CO3溶液的质量关系如图所示(恰好完全反应时所得食盐溶液仍为不饱和溶液)。
求:⑴井盐中CaCl2的质量分数;
⑵恰好完全反应后所得溶液中NaCl的质量分数(结果都保留一位小数)。
【答案】(1)48.7%;(2)11.7%
【解析】⑴解∶设井盐中CaCl2的质量为xg,反应生成氯化钠质量为yg,生成沉淀zg
Na2CO3 + CaCl2 =CaCO3↓+2NaCl
106 71 100 117
10.6%×100g x z y
![]() =
=![]() ,x=7.1g. 井盐中CaCl2的质量分数∶
,x=7.1g. 井盐中CaCl2的质量分数∶![]() ×100%=48.7%;
×100%=48.7%;
![]() =
=![]() ,y=11.7g.
,y=11.7g. ![]() =
=![]() ,z=10g.
,z=10g.
⑵恰好完全反应后所得溶液中NaCl的质量分数∶![]() ×100%=11.7%.
×100%=11.7%.
答∶⑴井盐中CaCl2的质量分数是48.7%;
⑵恰好完全反应后所得溶液中NaCl的质量分数是11.7%.
点睛∶本题主要考查质量守恒定律的应用以及根据化学方程式进行计算。

 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案【题目】我国约在南北朝时就开始冶炼黄铜,黄铜是铜和锌的合金(Cu-Zn),它可用来制造电器零件及日用品。小华利用一瓶稀盐酸和相关的仪器,测定黄铜样品的组成(不考虑黄铜中的其他杂质)。将30mL稀盐酸分三次加入到10g黄铜样品粉末中,每次充分反应后,测定生成氢气的质量,实验数据见下表:
第一次 | 第二次 | 第三次 | |
连续加入盐酸的体积/mL | 10 | 10 | 10 |
生成氢气的质量/g | 0.08 | X | 0.04 |
(1)X=____________;
(2)从上表数据分析,小华用10 g合金粉末总共收集到氢气_______g;
(3)求该合金中铜的质量分数。