题目内容
【题目】下图是甲、乙、丙三种固体物质的溶解度曲线,下列说法正确的是
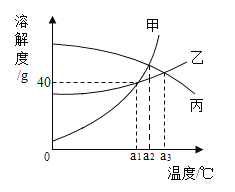
A.a2℃时,三种物质的溶解度由大到小的顺序是:甲=乙>丙
B.乙中含有少量甲时,可用冷却热饱和溶液的方法提纯乙
C.a1℃时,将30g乙加入50g水中充分溶解,所得溶液中溶质与溶剂的质量比为2:5
D.将a3℃甲、乙、丙三种物质的饱和溶液分别降温至a℃,所得溶液的溶质质量分数由大到小的顺序是:甲>丙>乙
【答案】CD
【解析】
A、a2℃时,三种物质的溶解度由大到小的顺序是:甲=丙>乙,不符合题意;
B、甲物质溶解度随温度变化大,适合用降温结晶法,乙物质溶解度随温度变化小,适合用蒸发结晶法,甲中含有少量乙时,可用冷却热饱和溶液的方法提纯甲,不符合题意;
C、a1℃时乙物质的溶解度为40g,即该温度下50g水中最多溶解20g乙,所得溶液中溶质与溶剂的质量比为2:5,符合题意;
D、将a3℃时甲、乙、丙三种物质的饱和溶液降温到a2℃时,甲、乙的溶解度减小,丙的溶解度随温度的降低而增大,甲、乙有晶体析出,质量分数变小溶液仍为饱和溶液,丙没有晶体析出,质量分数不变,一定温度下饱和溶液的溶质质量分数=![]() ,溶解度越大,质量分数越大,a2℃时甲的溶解度大于a3℃时丙的溶解度大于a2℃时乙的溶解度,所以a2℃时,三种物质的溶质质量分数由大到小的顺序是甲>丙>乙。故选CD。
,溶解度越大,质量分数越大,a2℃时甲的溶解度大于a3℃时丙的溶解度大于a2℃时乙的溶解度,所以a2℃时,三种物质的溶质质量分数由大到小的顺序是甲>丙>乙。故选CD。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】有一包白色固体,可能含有氯化钠、碳酸钠、硫酸钠和硝酸钡中的一种或几种。为探究固体的组成,某化学兴趣小组进行了如下所示实验:
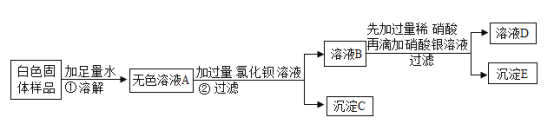
请回答下列问题:
(1)①和②都用到玻璃棒,但其作用不同。操作②中玻璃棒的作用是_____。
(2)原固体中一定不含有的物质是____(写物质名称)。
(3)为确定白色固体样品中可能存在的物质,小强对沉淀C进行实验:
实验操作 | 现象 | 结论 |
取少量沉淀C于试管中,加入过量稀硝酸 | ________ | 白色固体中有碳酸钠,没有硫酸钠 |
(4)小明同学认为白色固体中还不能确认是否存在的是_______,理由是(用化学方程式表示):________;如要说明肯定有该物质,只需将上述实验方案中所加的一种试剂改为________即可。