题目内容
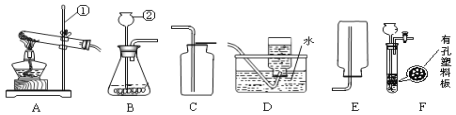
【题目】小红打算用下图完成实验室制取气体,请根据题目要求答题
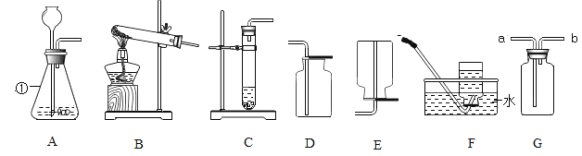
(1)写出标号仪器名称① ;
(2)实验室利用B装置制取氧气,写出该反应的文字或符号表达式为 要收集较纯净的氧气,应选择的收集装置是 (填编号,下同),如果用G装置来收集氧气则应从 端通入(填“a”或“b”)
(3)已知二氧化碳密度比空气大,能溶于水,在实验室可以利用稀盐酸(液体)和块状大理石混合制取二氧化碳,则可以选择的装置组合是 ;
(4)利用下图甲装置探究“MnO2的用量对 H2O2分解反应的影响”,实验中H2O2的溶质质量分数为3%,装置中产生氧气的量可以用压强传感器测出(在等温条件下,产生氧气体积与装置内压强成正比.反应放热忽略不计.)
①写出装置甲中的文字或符号表达式: ;
②图乙是“0.1克MnO2与不同体积的3%H2O2溶液混合”的实验结果,从图中可以得出的结论是 ;
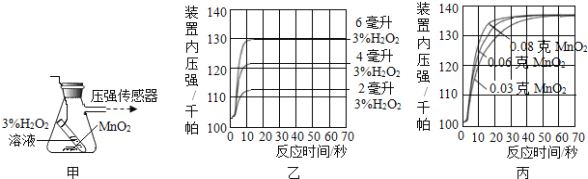
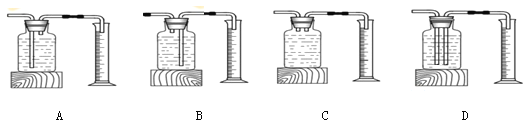
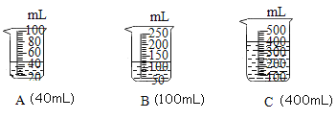
③当用“3%H2O2溶液8毫升与不同质量的MnO2混合”时,得到如图丙所示的曲线.曲线的斜率显示,当MnO2的用量增加到0.08克时,分解速度达到实验要求.在此实验条件下,若MnO2的质量有4克(一药匙),就能使如图 (选填字母)烧杯中所装的3%H2O2溶液,其分解速度最接近实验要求.
【答案】(1)①锥形瓶
(2)2KMnO4![]() K2MnO4+MnO2+O2↑,F;a
K2MnO4+MnO2+O2↑,F;a
(3)AD(4)①2H2O2![]() 2H2O+O2↑②过氧化氢溶液体积越大,产生氧气越多③C
2H2O+O2↑②过氧化氢溶液体积越大,产生氧气越多③C
【解析】
试题分析:实验室利用B装置制取氧气,写出该反应的文字或符号表达式为2KMnO4![]() K2MnO4+MnO2+O2↑;要收集较纯净的氧气,应选择的收集装置是F,如果用G装置来收集氧气则应从a端进入,因为氧气的密度大于空气;在实验室可以利用稀盐酸(液体)和块状大理石混合制取二氧化碳,则可以选择的装置组合是AD,因为不要加热所以发生装置为A,二氧化碳密度大于空气,所以用想上排气法收集;实验结果,从图中可以得出的结论过氧化氢溶液体积越大,产生氧气越多;图乙是“0.1克MnO2与不同体积的3%H2O2溶液混合”的实验结果,从图中可以看出H2O2的用量越多,产生的氧气越多;当用“3%H2O2溶液8毫升与不同质量的MnO2混合”时,得到如图丙所示的曲线。曲线的斜率显示,当MnO2的用量增加到0.08克时,分解速度达到实验要求,说明二者在比例为100:1的情况下反应最好。因此当MnO2的质量有4克时,过氧化氢的质量最好为400毫升。故选C。
K2MnO4+MnO2+O2↑;要收集较纯净的氧气,应选择的收集装置是F,如果用G装置来收集氧气则应从a端进入,因为氧气的密度大于空气;在实验室可以利用稀盐酸(液体)和块状大理石混合制取二氧化碳,则可以选择的装置组合是AD,因为不要加热所以发生装置为A,二氧化碳密度大于空气,所以用想上排气法收集;实验结果,从图中可以得出的结论过氧化氢溶液体积越大,产生氧气越多;图乙是“0.1克MnO2与不同体积的3%H2O2溶液混合”的实验结果,从图中可以看出H2O2的用量越多,产生的氧气越多;当用“3%H2O2溶液8毫升与不同质量的MnO2混合”时,得到如图丙所示的曲线。曲线的斜率显示,当MnO2的用量增加到0.08克时,分解速度达到实验要求,说明二者在比例为100:1的情况下反应最好。因此当MnO2的质量有4克时,过氧化氢的质量最好为400毫升。故选C。

【题目】区分下列各组物质所用的两种方法都正确的是 ( )
选项 | 需要区分的物质 | 方法一 | 方法二 |
A | 氯化铵与氯化钾 | 分别与熟石灰混合研磨 | 观察颜色 |
B | 食盐和纯碱 | 加食醋 | 溶解,滴加氯化钙溶液 |
C | 硝酸钠与亚硝酸钠 | 溶解,滴加酚酞试液 | 尝味道 |
D | 羊毛与涤纶 | 点燃,闻气味 | 观察色泽 |
【题目】除去下列物质中的少量杂质,所选用的试剂或操作方法错误的是
选项 | 物质 | 杂质 | 试剂 | 操作方法 |
A | 氧化铜粉 | 碳粉 | 空气 | 在空气中灼烧 |
B | 氯化亚铁溶液 | 氯化铜 | 过量的铁粉 | 过滤 |
C | 氮气 | 水蒸气 | 足量生石灰 | 通过盛生石灰的干燥管 |
D | 氯化钠溶液 | 氯化钙 | 过量碳酸钠溶液 | 过滤 |