题目内容
(7分)汽车是现代生活中不可缺少的代步工具。请回答下列问题:
(1)汽车电路中的导线大都是铜制的,这是利用了金属铜的延展性和____________性。
(2)下列汽车配件及用品中,属于有机合成材料的是(填序号,下同)__________。

a.钢铁外壳 b.玻璃车窗 c.橡胶轮胎 d.羊毛座垫
(3)铁在潮湿的空气中容易锈蚀。
①汽车表面喷漆,可以延缓汽车的锈蚀,其防锈原理是隔绝____________和水。
②喷漆前需将铁制品放入稀盐酸中除锈(铁锈主要成分是Fe2O3),观察到溶液变黄,有无色气泡逸出,反应的化学方程式是___________;___________。
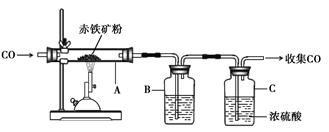
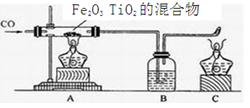
(4)回收再利用生锈的铁制品是保护金属资源的一种有效途径。右图所示的废铁粉中Fe2O3含量大约在80%(其余20%为铁)左右,回收后在工业上常用一氧化碳将其还原,反应的化学方程式是_______________,若回收100 t这样的废铁粉可以得到__________t铁。
(1)汽车电路中的导线大都是铜制的,这是利用了金属铜的延展性和____________性。
(2)下列汽车配件及用品中,属于有机合成材料的是(填序号,下同)__________。

a.钢铁外壳 b.玻璃车窗 c.橡胶轮胎 d.羊毛座垫
(3)铁在潮湿的空气中容易锈蚀。
①汽车表面喷漆,可以延缓汽车的锈蚀,其防锈原理是隔绝____________和水。
②喷漆前需将铁制品放入稀盐酸中除锈(铁锈主要成分是Fe2O3),观察到溶液变黄,有无色气泡逸出,反应的化学方程式是___________;___________。
(4)回收再利用生锈的铁制品是保护金属资源的一种有效途径。右图所示的废铁粉中Fe2O3含量大约在80%(其余20%为铁)左右,回收后在工业上常用一氧化碳将其还原,反应的化学方程式是_______________,若回收100 t这样的废铁粉可以得到__________t铁。

(1)导电 (2)c
(3)①空气(或氧气) ② Fe2O3 + 6HCl ="=" 2FeCl3 + 3H2O Fe + 2HCl ="=" FeCl2 + H2↑
(4)Fe2O3 + 3CO 2Fe + 3CO2(写加热给分) 76
2Fe + 3CO2(写加热给分) 76
(3)①空气(或氧气) ② Fe2O3 + 6HCl ="=" 2FeCl3 + 3H2O Fe + 2HCl ="=" FeCl2 + H2↑
(4)Fe2O3 + 3CO
 2Fe + 3CO2(写加热给分) 76
2Fe + 3CO2(写加热给分) 76试题分析:(1)金属具有优良的导热性、延展性和导电性等性能,其中,铜的导电性仅次于银,是一种很好的导电材料,故导线是利用其导电性;
(2)根据材料的分类及物质的组成进行判断:a钢铁属于金属材料,b玻璃属于硅酸盐材料,c橡胶轮胎属于有机合成材料,d羊毛属于天然材料,故选c。
(3)①铁生锈是铁在氧气和水的共同作用下发生的,所以通常防止铁生锈采用的方法是保持干燥环境或在金属表面涂油漆、加镀层金属等以隔绝空气(或氧气);
②酸能与金属和金属氧化物反应,铁制品放入稀盐酸中除锈(铁锈主要成分是Fe2O3),观察到溶液变黄,说明盐酸与铁锈反应生成了氯化铁和水,故反应的化学方程式为Fe2O3+6HCl=2FeCl3+3H2O;有无色气泡逸出,说明铁与盐酸发生了反应生成氯化亚铁和氢气,故反应的化学方程式为Fe+2HCl═FeCl2+H2↑。
(4)根据已有知识可知,一氧化碳与三氧化二铁在高温下反应,生成铁和二氧化碳,故反应的化学方程式为Fe2O3 + 3CO
 2Fe + 3CO2;
2Fe + 3CO2;根据题意可知,100t废铁粉中含有铁100×20%=20t,含有三氧化二铁为80t。
设80t三氧化二铁和CO反应生成铁的质量为x
Fe2O3 + 3CO
 2Fe + 3CO2
2Fe + 3CO2160 112
80t x
160:112=80t:x
解之得:x=56t
所以可以得到铁的质量为20t+56t=76t
点评:本题是以新情境为依托,对化学知识的考查,涉及的知识点较多,包含了化学方程式的计算,这就要求学生在平时的学习中要加强相关化学知识的储备,以便在解题时灵活应用。

练习册系列答案
 能力评价系列答案
能力评价系列答案 唐印文化课时测评系列答案
唐印文化课时测评系列答案
相关题目