题目内容
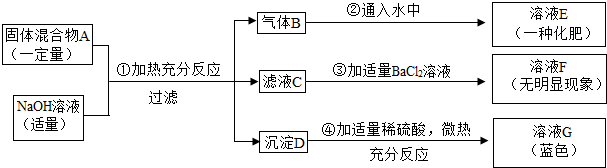
固体A中可能含有Na2SO4、FeCl3、Na2CO3、KCl中的一种或几种,进行如下实验,观察、记录现象,并逐步推出结论.请完成下表:①②③④| 实验步骤及现象 | 结论 |
| ①将少许A溶于水得到无色溶液B. | A中一定没有_____ |
| ②在B加入足量BaCl2溶液,生成白色沉淀C,过滤得滤液D. | A中一定有_______ ___________ |
| ③在C中加入足量稀硝酸,C部分溶解;在D中加入AgNO3溶液,生成的白色沉淀不溶于稀硝酸. | |
| ④另取少许A进行颜色反应,通过蓝色钴玻璃片,观察到火焰呈_____色. | A 中还有KCl |
【答案】分析:①FeCl3溶液是棕黄色的,可以排除FeCl3,②③加入氯化钡溶液生成白色沉淀,且沉淀在加入稀硝酸后部分溶解,说明沉淀为碳酸钙和硫酸钙,滤液D中有氯离子,加入硝酸银溶液后生成白色沉淀且不溶于稀硝酸,说明沉淀为氯化银,④根据焰色反应的原理,“焰色反应是某些金属或它们的挥发性化合物在无色火焰中灼烧时使火焰呈现特征的颜色的反应”推断火焰颜色.
解答:解:①因为FeCl3溶液是棕黄色,固体A溶液水得到的是无色溶液,故可判断A中一定没有FeCl3;
②③在B中加入氯化钡溶液后生成白色沉淀C,在C中加入稀硝酸,沉淀部分溶解,说明C中有碳酸钡沉淀和硫酸钡沉淀.因为碳酸钡沉淀可溶于稀硝酸,而硫酸钡沉淀不溶于稀硝酸;氯化钡与Na2CO3反应生成碳酸钡沉淀,与Na2SO4反应生成硫酸钡沉淀,由此可以判断A中一定有Na2CO3和Na2SO4;在滤液D中加入硝酸银溶液,生成氯化银沉淀(因为氯化银沉淀不溶于稀硝酸),说明溶液中一定有氯离子;
④因为KCl在焰色反应中呈现紫色,故可以观察到火焰呈紫色.
故答案为:①FeCl3;②③Na2SO4、Na2CO3;④紫.
点评:要正确解答本题,须知FeCl3溶液是棕黄色的,碳酸钡沉淀可溶于硝酸,硫酸钡沉淀和氯化银沉淀不溶于硝酸,钾的焰色反应为紫色.
解答:解:①因为FeCl3溶液是棕黄色,固体A溶液水得到的是无色溶液,故可判断A中一定没有FeCl3;
②③在B中加入氯化钡溶液后生成白色沉淀C,在C中加入稀硝酸,沉淀部分溶解,说明C中有碳酸钡沉淀和硫酸钡沉淀.因为碳酸钡沉淀可溶于稀硝酸,而硫酸钡沉淀不溶于稀硝酸;氯化钡与Na2CO3反应生成碳酸钡沉淀,与Na2SO4反应生成硫酸钡沉淀,由此可以判断A中一定有Na2CO3和Na2SO4;在滤液D中加入硝酸银溶液,生成氯化银沉淀(因为氯化银沉淀不溶于稀硝酸),说明溶液中一定有氯离子;
④因为KCl在焰色反应中呈现紫色,故可以观察到火焰呈紫色.
故答案为:①FeCl3;②③Na2SO4、Na2CO3;④紫.
点评:要正确解答本题,须知FeCl3溶液是棕黄色的,碳酸钡沉淀可溶于硝酸,硫酸钡沉淀和氯化银沉淀不溶于硝酸,钾的焰色反应为紫色.

练习册系列答案
 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案
相关题目