��Ŀ����
����Ŀ���ڡ���ۡ����ۡ������š�֮�佨����ϵ���ǻ�ѧѧ�Ƶ��ص㡣
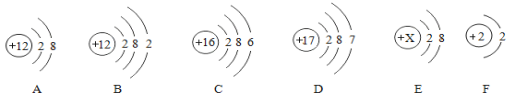
��1��

�������ڻ�������__�����ڵ��ʵ���____��
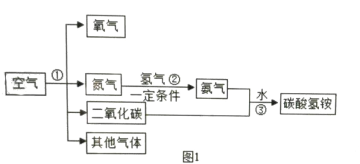
��2�������DZ������Ȼ��Դ����ͼ1��ʾ���Կ���Ϊ��Ҫԭ�Ϻϳ�̼����泥�NH4HCO3�������̡��밴Ҫ��ش��������⣺
�ٲ���ٵõ��ġ��������塱����Ҫ�ɷ���__________��
����ͼ2���Ա�ʾ����ڵķ�Ӧ���̣�
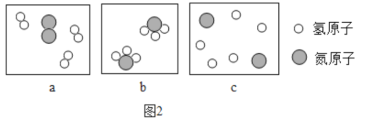
a�ӷ�Ӧ��ʼ����ɵ�����˳��Ϊ_______������ĸ����
bд�����������ʾ�ķ�Ӧ�Ļ�ѧ����ʽ__________��
�۲���۵ķ�Ӧ����__________���������Ӧ���ͣ���
��3����ˮ�����ۺͺ������������У��ɷ���ֱ�ӹ��ɵ������ǣ��ѧʽ��_____��
��4��ʳ����Լ��3%-5%�Ĵ��ᣨC2H4O2����������_____��Ԫ����ɣ�����̼Ԫ�غ���Ԫ�ص���������________�������Ħ������Ϊ _______��2mol C2H4O2������Ϊ_____g������Լ���� _____����ԭ�ӣ���____ g��ԭ�ӡ�
���𰸡��� �ҡ��� ϡ������ acb 3H2+N2![]() 2NH3 ���Ϸ�Ӧ H2O 3 3��4 60g/mol 120 2.408��1024 8
2NH3 ���Ϸ�Ӧ H2O 3 3��4 60g/mol 120 2.408��1024 8
��������
��1�����������ʵ���ʾ��ģ�ͣ����ж����ɲ�ͬ�ַ��ӹ��ɵģ����ڻ���������ͬ�ֵķ��ӹ��ɵģ����ڻ��������ҡ�������ͬ�ֵ�ԭ��ֱ�ӹ��ɵģ����ڵ�����
��2���ٿ����и��ɷֵ���������ֱ��ǣ�������Լռ78%��������Լռ21%��ϡ�������Լռ0.94%��������̼��Լռ0.03%��ˮ������������������ʴ�Լռ0.03%�����Բ�����еõ�������������������Ҫ�ɷ���Ϊ��ϡ�����壻
��a��������������ģ��ͼ��ʾ������з�Ӧ���̣��������������ɰ������Ƿ����ȷֳ�ԭ�ӣ�ԭ��������ϣ���ӷ�Ӧ��ʼ����ɵ�����˳��Ϊacb��
b�����������ʾ�ķ�Ӧ�ǵ�����������һ�������·�Ӧ���ɰ�������Ӧ�Ļ�ѧ����ʽ��3H2+N2 ![]() 2NH3 ��
2NH3 ��
�۲�����ǰ�����ˮ�Ͷ�����̼��Ӧ����̼����泥��÷�Ӧ���ڻ��Ϸ�Ӧ��
��3��ˮ����ˮ���ӹ��ɵģ��������ڽ������ʣ�������ԭ��ֱ�ӹ��ɵģ��������ڹ�̬�ǽ������ʣ�����̼ԭ��ֱ�ӹ��ɵģ�
��4��������̼Ԫ�ء���Ԫ�غ���Ԫ�ص�3��Ԫ����ɣ�̼����Ԫ�ص�������Ϊ����12��2������16��2��=3��4��Ħ��������ָ��λ���ʵ��������������е��������������Է�������Ϊ12��2+1��4+16��2=60���ʴ����Ħ��������60g/mol��2molC2H4O2������=2��60g/mol=120g��2mol���������Լ�����������Ϊ2��6.02��1023��һ��������Ӻ���2����ԭ�ӣ���2molԼ����������2��2��6.02��1023=2.408��1024����ԭ�ӣ�������ԭ�ӵ�����=120g��![]() =8g��
=8g��

 ��У����ϵ�д�
��У����ϵ�д�����Ŀ�������Ͷ����о����ڻ�ѧ��ѧ��չ���ش����ã���ش��������⡣
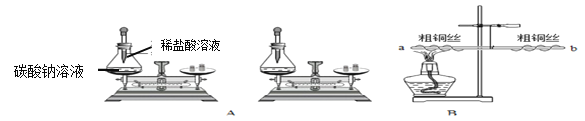
��1���������̶Թ�������ķֽ��д����ã��ֽ�34g����������Һ�ڷ�Һ©��A�У���B�м���һ�����Ķ������̣�����K���ִ���ͬʱ�������ƽ�Ķ������±���ʾ��������H2O�ݳ�����
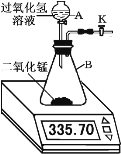
��Ӧʱ�䣯min | 0 | 1 | 2 | 3 | 4 | 5 | 6 |
װ�� + ����������Һ + ��������/g | 335.70 | 333.78 | 332.64 | 332.58 | 332.50 | 332.50 | 332.50 |
����Ŀ��֪��������������Ϊ__________
��������������������μӷ�Ӧ�Ĺ�����������ʵ��������ݻ�ѧ����ʽ��ʽ���㣩________
��2��С��ͬѧ����FeCl3��Һ��CuSO4��Һ�Թ�������ķֽ�Ҳ�д����ã�Ϊ�Ƚ���ͬŨ�ȵ�FeCl3��Һ��CuSO4��Һ�Թ�������ֽ�Ĵ�Ч����������������̽����
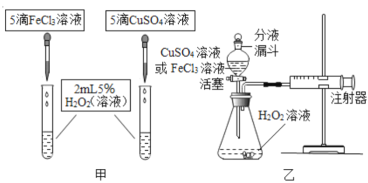
������̽����
��ͼ�ף���ͨ���۲�_______�����ԱȽ����ߵĴ�Ч������ʱ�Ա�ʵ��Ӧ���Ƶ���ͬ������____________��
���������
��ͼ�ң�Ҫ�����Ƚ����ߵĴ�Ч�����ɲ������ɵ���������_________��ʵ��ǰҪ������___________��