题目内容
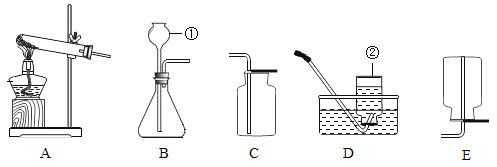
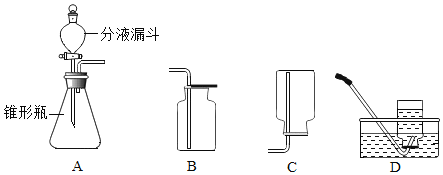
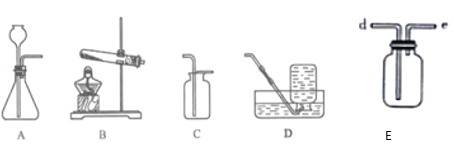
【题目】下图是实验室制取气体的发生装置和气体收集装置.请你回答下列问题:
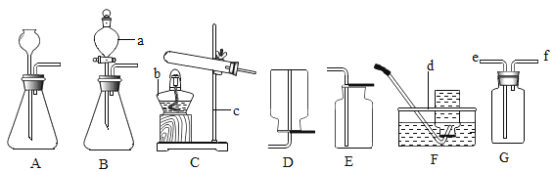
(1)写出标号仪器名称:a__________、b__________
(2)实验室用过氧化氢溶液制取氧气,其反应的化学方程式是_________,若从控制反应效率和节约药品的角度考虑,应选择的发生装置是________(填字母编号).
(3)实验室若用氯酸钾和二氧化锰(作催化剂)制取氧气,可选择装置C作发生装置,其反应的化学方程式是_________.如果用高锰酸钾制取氧气,装置C还需做的一点改动是__________,这样改动的原因是:___________.
(4)D、E、F、G都是实验室中气体的收集装置,其中不能用来收集氧气的是__________(填字母编号).
(5)与集气瓶配套使用的玻璃片一般一面为光滑面,另一面为磨砂面,收集气体时用玻璃片的__________盖好集气瓶(填“光滑面”或“磨砂面”).
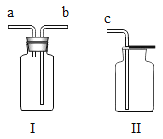
(6)若用上图所示的G装置收集氧气,验满时,应将带火星的木条放在__________(填“e”或“f”)端导口,若复燃,说明氧气已满.
(7)在“氧气的制取和性质”实验中,某同学取一段纱窗网上的细铁丝,绑上火柴.绑火柴的作用是______,将铁丝绕成螺旋状是为了__________;然后在自己收集的氧气中做“铁丝在氧气中燃烧”的实验,结果没有观察到“火星四射”的现象.请分析此实验失败可能的原因________(写出两条即可).
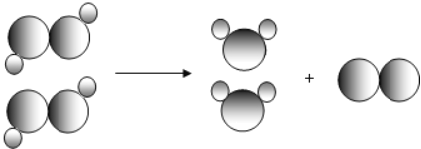
(8)某化学兴趣小组借助氧气传感器探究微粒的运动,数据处理软件可实时绘出氧气体积分数随时间变化的曲线。收集一塑料瓶氧气进行以下三步实验:①敞口放置;②双手贴在塑料瓶外壁上;③将塑料瓶的瓶口朝下,三步实验中测得氧气的体积分数随时间变化的曲线依次为图2中的MN段、NP段和PQ段。

①能够说明氧分子不断运动的曲线是_____(填字母)。
A MN段 B NP段 C PQ段
②NP段和MN段相比较,说明_____。
③随着实验的进行,传感器测出氧气的体积分数约为_______ 时几乎不再变化。
【答案】分液漏斗 酒精灯 2H2O2![]() 2H2O+O2↑ B 2KClO3
2H2O+O2↑ B 2KClO3![]() 2KCl+3O2↑ 试管口塞一团棉花 防止高锰酸钾粉末进入导管,堵塞导管 D 磨砂面 f 引燃铁丝 增大铁丝受热面积 铁丝上有铁锈;氧气的浓度太低等 A 温度越高,分子运动越快 21%
2KCl+3O2↑ 试管口塞一团棉花 防止高锰酸钾粉末进入导管,堵塞导管 D 磨砂面 f 引燃铁丝 增大铁丝受热面积 铁丝上有铁锈;氧气的浓度太低等 A 温度越高,分子运动越快 21%
【解析】
(1)仪器a的名称是分液漏斗,仪器b的名称是酒精灯;
(2)过氧化氢在二氧化锰的催化作用下分解生成水和氧气,化学方程式为:2H2O2![]() 2H2O+O2↑,分液漏斗可以控制液体的滴加速度,所以从控制反应速率和节约药品的角度考虑,应选择的发生装置是B;
2H2O+O2↑,分液漏斗可以控制液体的滴加速度,所以从控制反应速率和节约药品的角度考虑,应选择的发生装置是B;
(3)氯酸钾在二氧化锰的催化作用下加热生成氯化钾和氧气,化学方程式为:2KClO3![]() 2KCl+3O2↑;如果用高锰酸钾制取氧气,装置A还需做的一点改动是在试管口塞一团棉花,这样改动的原因是,这样改动的原因是防止高锰酸钾粉末进入导管,堵塞导管;
2KCl+3O2↑;如果用高锰酸钾制取氧气,装置A还需做的一点改动是在试管口塞一团棉花,这样改动的原因是,这样改动的原因是防止高锰酸钾粉末进入导管,堵塞导管;
(4)氧气的密度比空气大,所以不能用D来收集氧气;
(5)磨砂处理是让化学器具之间的接触面更光滑、接合更紧的一种方法,与集气瓶配套使用的玻璃片一般一面为光滑面,另一面为磨砂面,收集气体时应用玻璃片的磨砂面盖好集气瓶;
(6)若用G装置收集氧气,由于气体的密度比空气的密度大,故由e进入,由f流出,所以验满时,应将带火星的木条放在f导口,若木条复燃,说明氧气已满;
(7)铁丝在氧气中燃烧时绑上火柴,绑火柴的作用是引燃铁丝;将铁丝绕成螺旋状是为了增大铁丝受热面积;在收集的一瓶氧气中做“铁丝在氧气中燃烧”的实验,结果没有观察到“火星四射”的现象,原因可能是:铁丝上有铁锈;氧气的浓度太低等;
(8)图2中,①能够说明氧分子不断运动的曲线是MN段,因为是瓶口向上敞口放置,故选A;②MN段和NP段相比较,说明:温度越高,分子运动越快;③随着实验的进行,传感器测出氧气的体积分数约为21%时几乎不再变化,因为氧分子扩散趋向平衡;故答案为:①A;②温度越高,分子运动越快;③21%;

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】NaCl和KNO3在不同温度时的溶解度如下,回答下列问题:
温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | |
溶解度/g | NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 |
KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.8 | 110 | |
(1)如图为NaCl和KNO3的溶解度曲线,则表示NaCl的溶解度曲线是________(填“甲”或“乙”);其中温度t的范围应在________(填字母序号)。
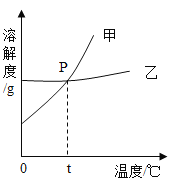
A 10℃~20℃之间 B 20℃~30℃之间 C 30℃40℃之间 D 40℃~50℃之间
(2)若甲物质中含有少量的乙物质,提纯甲物质的方法是________。
(3)在0℃时,分别在100g水中加入30g NaCl和KNO3固体,再加热到60℃时(假设溶剂不损耗),加热前后,有关两种溶液的说法正确的是________(填字母序号)。
A 0℃时,两溶液中溶质的质量分数相同
B 60℃时两溶液中溶质的质量分数相同
C 加热前后,NaCl溶液中溶质的质量分数由小变大
D 加热前后,KNO3溶液中溶质的质量分数不变