题目内容
【题目】为了使经济可持续发展,生产过程应尽量减少对环境的负面作用。由单质铜制取硫酸铜有下列几种步骤,其中可行且符合以上要求的是( )
A.Cu→CuSO4B.Cu→CuO→CuSO4
C.Cu→Cu2(OH)2CO3→CuSO4D.Cu→Cu(NO3)2→Cu(OH)2→CuSO4
【答案】B
【解析】
A、Cu→CuSO4,因为铜和稀硫酸不反应,只能和Ag2SO4反应生成硫酸铜,但是Ag2SO4溶解度很小,而且Ag2SO4不是常见的试剂,造价成本太高。所以A不行;
B、制得的方法是:2Cu+O2![]() 2CuO、CuO+H2SO4═CuSO4+H2O,反应原料易得,没有污染,符合要求;
2CuO、CuO+H2SO4═CuSO4+H2O,反应原料易得,没有污染,符合要求;
C、铜生成碱式碳酸铜的反应很慢,这个方法不适用,此项错误;
D、此方案需要多步反应,操作复杂,且由铜制取硝酸铜,一般是铜和硝酸银反应,也不经济,故此项错误。
故选B。

 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案【题目】用“盐酸—硫酸钡法”生产BaCl2会放出有毒气体H2S(其水溶液有酸性),可用NaOH吸收H2S制取Na2S进行处理。(相关反应的化学方程式:H2S+2NaOH=Na2S+2H2O)
项目 | 单价(元/吨) |
NaOH | 2500 |
Na2S | 5000 |
辅助费用(以处理1吨H2S计) | 1114 |
(1)若某化工厂每天要处理10吨H2S,需消耗NaOH多少吨_____?
(2)下表为H2S回收工艺的各项生产成本:
根据上述资料分析,从经济效益考虑这种处理H2S的方法是___(选填“盈利”或“亏损”)的。
【题目】请从 A 或B 两题中任选一个作答,若两题均作答,按 A 计分。
在一定条件下,Mg 和 MgH2的相互转化可以实现氢气的储存和释放。其工作原理如图。
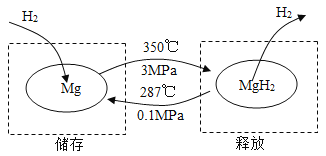
A | B |
(1)氢气储存时发生反应的化学方程式为_______。 (2)氢气很容易逃逸,若氢气存储效率为 10%,储存 1 kg 氢气,至少需要 Mg 的质量为_______ kg。 | (1)氢气释放时发生反应的化学方程式 为_______。 (2)理论上,52 kg MgH2最多能释放氢气的质量为_______ kg。 |