题目内容
【题目】黄铜是铜和锌的合金,某化学兴趣小组为研究合金中铜的含量,取样品 15g进行如下操作。
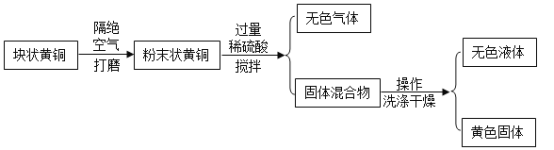
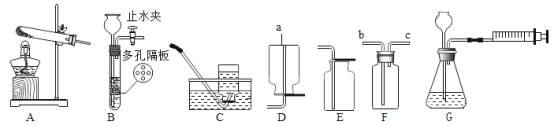
(1)操作①的名称是_____。该操作用到的玻璃仪器有玻璃棒、烧杯、_____。
(2)加入稀硫酸发生的反应的化学方程式为_____。
(3)最后称得黄色固体为 13g,得到含铜量为 86.7%,高于实际含铜量,其原因可能是_____。
【答案】过滤 漏斗 Zn+H2SO4═ZnSO4+H2↑ 由于铜覆盖在锌的表面,使锌不能完全参加反应(或黄铜没有研磨得足够细,使部分锌没有参加反应)
【解析】
(1)根据过滤的原理和操作分析回答;
(2)根据锌能与稀硫酸反应写出反应的化学方程式;
(3)根据生成的铜覆盖在锌的表面分析回答。
(1)操作①能将固液分开,名称是过滤,该操作用到的玻璃仪器有玻璃棒、烧杯、漏斗。故填:过滤,漏斗。
(2)加入稀硫酸发生的反应的是锌与稀硫酸反应生成了硫酸锌和氢气,化学方程式为:Zn+H2SO4═ZnSO4+H2↑,故填:Zn+H2SO4═ZnSO4+H2↑。
(3)最后称得黄色固体为13g,得到含铜量为86.7%,高于实际含铜量,其原因可能是:由于铜覆盖在锌的表面,使锌不能完全反应(或黄铜没有研磨得足够细,使部分锌没有参加反应)。故填:由于铜覆盖在锌的表面,使锌不能完全参加反应(或黄铜没有研磨得足够细,使部分锌没有参加反应)。

 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案【题目】实验课上,某小组的同学用块状生石灰进行“化学反应中能量的变化”实验时发现:向块状生石灰样品中加入适量水后没有明显的温度变化。为确定其原因,进行了如下实验探究。实验验证一。
[提出问题]生石灰是否变质?其成分是什么?
[查阅资料]氢氧化钙溶解过程中无明显温度变化,与盐酸反应无气体生成。
[猜想与假设]同学们认为块状生石灰样品已变质,并对其成分作出了如下4种猜想。
猜想1:氧化钙和氢氧化钙:猜想2:氧化钙和碳酸钙:猜想3:______________;
猜想4:氧化钙、氢氧化钙和碳酸钙。
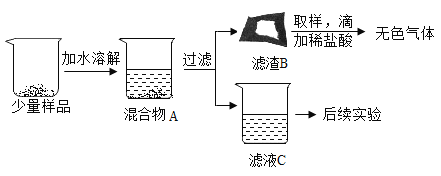
[进行实验]同学们将少量样品研碎后,按如图所示过程进行实验。
(1)在溶解过程中用温度计测量液体的温度,发现温度计示数升高,说明样品中应该含有______________。
[结论]猜想3不成立。
(2)滤渣B中一定含有_____________,用化学方程式表示变质过程中生成该物质的反应_____________。
[结论]①块状生石灰表面发生变质:②猜想1不成立。
(3)为验证滤液C的成分,进行后续实验。
实验操作 | 实验现象 | 实验结论 |
____________ | ____________ | ② 滤液中溶质为氢氧化钙 ②猜想4成立,猜想2不成立 |
[反思与评价]
(4)有的同学认为上述实验过程不能得出猜想4成立、猜想2不成立的结论,理由是______________。
[注意:答对15题以下小题奖励4分,化学试卷总不超过60分]
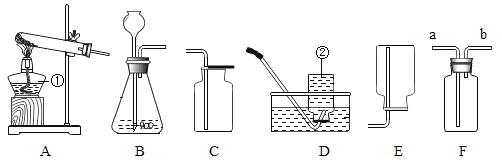
实验验证二:为了进一步确定块状生石灰样品的成分及质量,实验小组利用如下图所示的装置(夹持仪器省略)进行实验。
查阅资料:氢氧化钙加热至580°C、碳酸钙加热至825°C分别分解生成两种氧化物。
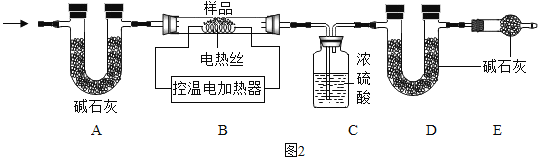
(5)①装置E的作用是______________。
②控温电加热器使装置B中反应完全,再通一段时间空气,测得反应前后装置C、D分别增重18.0g和22.0g,将装置B中反应后剩余的固体氧化物加入足量水中溶解,蒸发所得固体(不含水)增重36. 0g.求原块状生石灰固体样品中各成分为______________,各物质的质量______________。