题目内容
(2004?宿迁)某校课外活动小组模拟工业生产方法,用金属铜粉制取少量硫酸铜.请根据他们的实验操作,回答下面有关问题:(1)向盛有一定量稀硫酸的烧杯中,放入一定量的铜粉.此时铜粉的表面是否有气泡冒出?______ (填“是”或“否”)
(2)加热烧杯中的稀硫酸和铜粉时,烧杯底部应垫上______,使其受热______.
(3)如图所示(图中加热装置未画出):将导气管口对着铜粉连续不断地通入氧气.可以观察到铜粉逐渐减少,直至完全消失.写出此过程中所发生反应的化学方程式:______ 2CuO;CuO+H2SO4═CuSO4+H2O


【答案】分析:(1)铜的金属性排在氢后,不能与酸反应;
(2)烧杯不能直接加热;
(3)金属能与氧气反应生成金属氧化物,金属氧化物与酸能反应生成盐和水;
(4)蒸发时要用玻璃棒搅拌使液体受热均匀.
解答:解:
(1)铜的金属性排在氢后,不能与酸反应;
(2)烧杯不能直接加热,应垫石棉网,使其受热均匀;
(3)铜能与氧气反应生成氧化铜,氧化铜与稀硫酸能反应生成硫酸铜和水;
(4)蒸发时要用玻璃棒搅拌使液体受热均匀.
故答案为:
(1)否;
(2)石棉网,均匀;
(3)2Cu+O2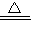 2CuO;CuO+H2SO4═CuSO4+H2O
2CuO;CuO+H2SO4═CuSO4+H2O
(4)玻璃棒,搅拌使液体受热均匀,
点评:此题考查的知识点较多,包括金属的活动性顺序、化学方程式的书写等;解决问题时要抓住实验的目的、实验的操作、实验的过程、实验的现象等方面,从基础入手.
(2)烧杯不能直接加热;
(3)金属能与氧气反应生成金属氧化物,金属氧化物与酸能反应生成盐和水;
(4)蒸发时要用玻璃棒搅拌使液体受热均匀.
解答:解:
(1)铜的金属性排在氢后,不能与酸反应;
(2)烧杯不能直接加热,应垫石棉网,使其受热均匀;
(3)铜能与氧气反应生成氧化铜,氧化铜与稀硫酸能反应生成硫酸铜和水;
(4)蒸发时要用玻璃棒搅拌使液体受热均匀.
故答案为:
(1)否;
(2)石棉网,均匀;
(3)2Cu+O2
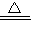 2CuO;CuO+H2SO4═CuSO4+H2O
2CuO;CuO+H2SO4═CuSO4+H2O(4)玻璃棒,搅拌使液体受热均匀,
点评:此题考查的知识点较多,包括金属的活动性顺序、化学方程式的书写等;解决问题时要抓住实验的目的、实验的操作、实验的过程、实验的现象等方面,从基础入手.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目

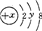 ,则x、y的值分别为( )
,则x、y的值分别为( )