题目内容
【题目】根据如图1装置图,回答有关问题. 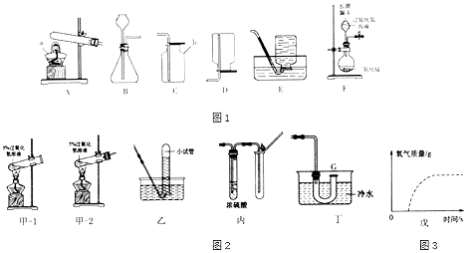
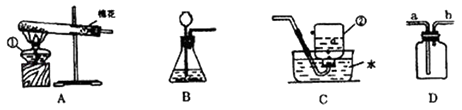
(1)写出装置图中标号仪器的名称:a , b .
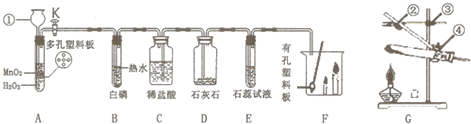
(2)写出实验室用高锰酸钾制取氧气的化学方程式 , 如图E装置来收集氧气,当导管口气泡放出时,再把导管口伸入盛满水的集气瓶,开始收集.
(3)写出实验室用过氧化氢溶液和二氧化锰制取氧气的化学方程式 , 可选用的发生装置是(填字母).选F作为发生装置错误的原因是 .
(4)资料显示,将新制的含H2O25%(即H2O2的质量除以溶液总质量×100%)的溶液,加热到80℃时,才有较多氧气产生,而相同质量含H2O25%的溶液加入催化剂,常温下就会立即产生氧气,反应速率快,所需时间短.
小晨按图2甲﹣1装置进行实验,当试管中有大量气泡出现时,用带火星的木条放在导管口,木条并未复燃,为此,他将乙和甲﹣2相连,利用图乙装置收集气体,再用带火星的木条检验,木条复燃,那么图甲实验中带火星木条未复燃的原因是 .
老师又设计了另一个改进的丙装置,将丙和甲﹣2相连后,用带火星的木条检验,木条也易复燃.请通过分析说出浓硫酸的作用 . 将丁和甲﹣2相连后,用带火星的木条在G处检验,木条(填能或不能)复燃.
(5)采用相同质量含H2O25%的溶液,图戊中虚线表示加热分解制取氧气的曲线,请你在该图3中用实线画出利用催化剂制取氧气的大致曲线(假定两种方法H2O2均完全分解,把曲线画在答题纸上).
【答案】
(1)酒精灯;集气瓶
(2)2KMnO4 ![]() K2MnO4+MnO2+O2↑;连续、均匀
K2MnO4+MnO2+O2↑;连续、均匀
(3)2H2O2 ![]() 2H2O+O2↑;B;长颈漏斗的下端未伸入液面以下
2H2O+O2↑;B;长颈漏斗的下端未伸入液面以下
(4)加热过氧化氢溶液的同时,溶液中的水蒸气随氧气一起逸出,环境湿度较大,氧气的量较少;吸收水蒸汽;能
(5)解:由于过氧化氢在二氧化锰催化作用下能分解放出氧气,所以,利用催化剂制取氧气的大致曲线为:

【解析】解:(1)图中标示仪器分别为:a是酒精灯,b是集气瓶;(2)高锰酸钾受热分解生成锰酸钾和二氧化锰和氧气,该反应的化学方程式为:2KMnO4 ![]() K2MnO4+MnO2+O2↑;如图E装置来收集氧气,当导管口气泡连续、均匀放出时,再把导管口伸入盛满水的集气瓶,开始收集;(3)过氧化氢和二氧化锰混合制取氧气可生成水和氧气,此反应是固液不加热反应,应该选用的发生装置是B,反应的方程式是2H2O2
K2MnO4+MnO2+O2↑;如图E装置来收集氧气,当导管口气泡连续、均匀放出时,再把导管口伸入盛满水的集气瓶,开始收集;(3)过氧化氢和二氧化锰混合制取氧气可生成水和氧气,此反应是固液不加热反应,应该选用的发生装置是B,反应的方程式是2H2O2 ![]() 2H2O+O2↑;选F作为发生装置错误的原因是:长颈漏斗的下端未伸入液面以下,生成的气体会从长颈漏斗中逸出;(4)图2甲﹣1实验中带火星木条未复燃的原因是:加热过氧化氢溶液的同时,溶液中的水蒸气随氧气一起逸出,环境湿度较大,氧气的量较少;浓硫酸具有吸水性,可以除去氧气中含有的水蒸气;将丁和甲﹣2相连后,水蒸气冷凝,得到干燥的氧气,故带火星的木条较易复燃;(5)由于过氧化氢在二氧化锰催化作用下能分解放出氧气,所以,利用催化剂制取氧气的大致曲线为:
2H2O+O2↑;选F作为发生装置错误的原因是:长颈漏斗的下端未伸入液面以下,生成的气体会从长颈漏斗中逸出;(4)图2甲﹣1实验中带火星木条未复燃的原因是:加热过氧化氢溶液的同时,溶液中的水蒸气随氧气一起逸出,环境湿度较大,氧气的量较少;浓硫酸具有吸水性,可以除去氧气中含有的水蒸气;将丁和甲﹣2相连后,水蒸气冷凝,得到干燥的氧气,故带火星的木条较易复燃;(5)由于过氧化氢在二氧化锰催化作用下能分解放出氧气,所以,利用催化剂制取氧气的大致曲线为:  ;故答案为:(1)酒精灯;集气瓶;(2)2KMnO4
;故答案为:(1)酒精灯;集气瓶;(2)2KMnO4 ![]() K2MnO4+MnO2+O2↑;连续、均匀;(3)B;2H2O2
K2MnO4+MnO2+O2↑;连续、均匀;(3)B;2H2O2 ![]() 2H2O+O2↑;长颈漏斗的下端未伸入液面以下;(4)加热过氧化氢溶液的同时,溶液中的水蒸气随氧气一起逸出,环境湿度较大,氧气的量较少;吸收水蒸汽;能;(5)
2H2O+O2↑;长颈漏斗的下端未伸入液面以下;(4)加热过氧化氢溶液的同时,溶液中的水蒸气随氧气一起逸出,环境湿度较大,氧气的量较少;吸收水蒸汽;能;(5) .
.
(1)根据常用仪器的名称与用途分析解答;(2)根据高锰酸钾受热分解生成锰酸钾和二氧化锰和氧气写出反应的化学方程式即可;根据用高锰酸钾制取氧气时的注意事项进行分析;(3)过氧化氢和二氧化锰混合制取氧气可生成水和氧气,反应不需加热选择发生装置;据反应原理书写方程式;根据长颈漏斗的使用注意事项分析;(4)根据在加热时水受热会蒸发分析;根据浓硫酸具有吸水性进行分析;根据两个装置的不同点进行分析;(5)根据过氧化氢在二氧化锰催化作用下能分解放出氧气分析.

 轻松暑假总复习系列答案
轻松暑假总复习系列答案