题目内容
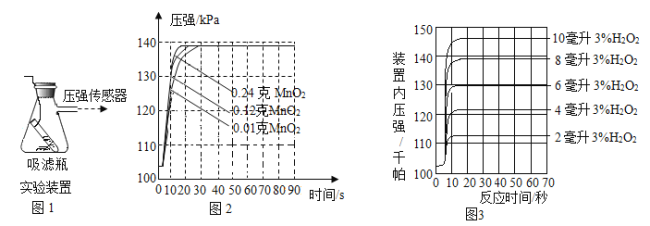
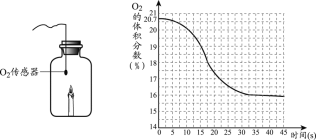
【题目】一定条件下,蜡烛在一瓶空气中燃烧。利用O2传感器,测定燃烧过程中O2的体积分数,变化如下图所示,下列说法不正确的是
A. 蜡烛燃烧需要氧气
B. 蜡烛熄灭后,密闭容器中还有氧气
C. 蜡烛燃烧前,密闭容器中氧气的体积分数小于21%
D. 蜡烛熄灭后,密闭容器中的二氧化碳体积分数为84%
【答案】D
【解析】
A、随着氧气减少到一定程度,蜡烛会熄灭,说明蜡烛燃烧需要氧气,该选项说法正确;
B、当氧气体积分数减小到16%时,蜡烛熄灭,说明蜡烛熄灭后,密闭容器中还有氧气,该选项说法正确;
C、由图中信息可知,蜡烛燃烧前,密闭容器中氧气的体积分数小于21%,该选项说法正确;
D、蜡烛熄灭后,密闭容器中的二氧化碳体积分数小于84%,这是因为空气中除去氧气和二氧化碳外,还含有稀有气体等物质,该选项说法不正确。
故选D。

【题目】在小英家的仓库里,堆放着一袋袋化肥一一碳酸氢铵( NH4HCO3).过了一个夏天,小英发现这种化肥所持有的刺激性气味变得更浓烈了,有些化肥袋里碳酸氢铵变少了,检查发现变少的化肥包装袋没有密封,化肥也没有撒落在地上,更没有人进过仓库开袋使用。
为了探究这些化肥减少的原因,小英在实验室取了一些碳酸氢铵粉末,放在蒸发皿中加热,过一会儿观察到粉末完全消失,同时也闻到了这种刺激性气味.粉末为什么会消失呢?
(1)(提出问题)碳酸氢铵粉末消失的原因是什么?
(2)(猜想)①碳酸氢铵粉末在不加热或加热条件下由固态变成它的气态。②碳酸氢铵在不加热或加热条件下发生分解反应,可能产生的物质有氨气和一些氧化物。
(3)(查阅资料)①碳酸氢铵属于氨肥,不具有升华的性质,说明上述猜想__________ (填序号)不成立;②氨气(化学式NH3)具有特殊的刺激性气味,极易溶于水,其水溶液是碱性,但干燥的氨气不能使干燥的红色石蕊试剂变蓝;③NO2为红棕色气体。NO为无色气体,在空气中易发生反应:2NO+O2=2NO2
(4)(实验操作,现象与结论)
实验操作 | 实验现象 | 实验结论 |
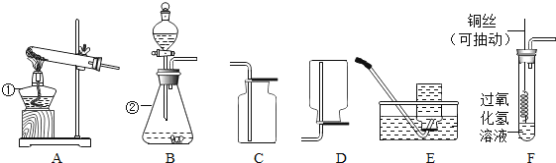
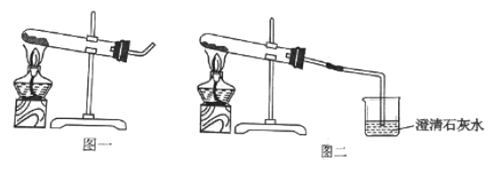
①取适量碳酸氢铵于试管中加热,如图一所示,将干燥的红色石蕊试纸接近导管口 | 产生强烈的刺激性气味,试管壁上有无色液滴且试纸变蓝,但未见红棕色气体 | 分解产物中有______,没有__________ |
②按如图二所示装置继续实验,直到反应完全 | 澄清石灰水变浑浊 | 分解产物中有__________ |
(5)(应用)①利用氨气的化学性质,请写出实验室检验氨气的方法(写出实验操作、现象、结论):________________________________________;
②如果你家里有碳酸氢铵化肥,你应该如何保存? ______________________________。
【题目】某兴趣小组同学对实验室制备氧气的条件进行如下探究实验。
(提出问题)①氧化铜是否也能作氯酸钾分解的催化剂?是否比二氧化锰催化效果更好?
(设计并完成实验)
I、将 3.0g 氯酸钾放在试管中加热
II、将 3.0g 氯酸钾与 1.0g 二氧化锰均匀混合加热
III、将 Xg 氯酸钾与 1.0g 氧化铜均匀混合加热
(实验现象分析)III 中 X 的值应为_____;将实验 I 和 III 比较可证明_____;
将实验反应后的固体加水溶解、过滤、洗涤、干燥,若称量得到 1.0g 黑色粉末,再将黑色粉末和 Xg 氯酸钾混合加热, 现象与实验 III 相同,此步骤是为了证明氧化铜在该化学反应前后_____和_____都不变;
(结论)氧化铜也能作氯酸钾分解的催化剂。
(实验反思)实验 II 和 III 对比是为了证明_____;
(提出问题)②双氧水分解速度还和什么因素有关。
(设计并完成实验)
实验 | 双氧水的质量 | 双氧水的浓度 | MnO2 的质量 | 相同时间内产生 O2 体积 |
1 | 50.0g | 1% | 0.1g | 9mL |
2 | 50.0g | 2% | 0.1g | 16mL |
3 | 50.0g | 4% | 0.1g | 31mL |
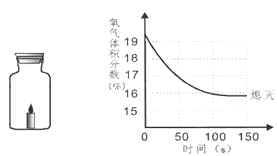
本实验中,测量 O2 体积的装置是_____(填编号)。
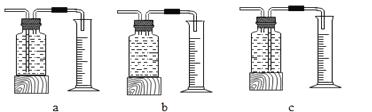
(结论)根据上表可知:在相同条件下,双氧水的浓度越大,双氧水分解的速率越_____。