题目内容
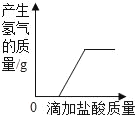
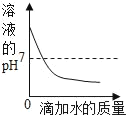
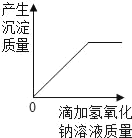
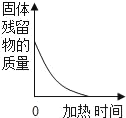
【题目】如图所示,某同学做了有关稀盐酸的化学性质实验。
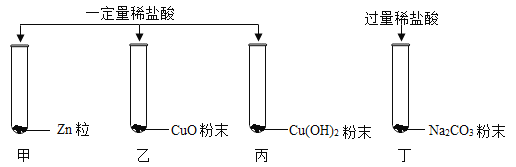
(1)甲试管中,发生反应的化学方程式为_____。
(2)四支试管,其中_____试管中的固体一定全部溶解。
(3)实验后将甲、乙、丙试管中的所有物质都倒入一个空烧杯中;稍后将丁试管中的物质倒入此烧杯中,有气泡产生。则:此气泡的气体物质是_____静置后,烧杯内上部的澄清液中的溶质一定含有_____。
【答案】Zn+2HCl═ZnCl2+H2↑ 丁 氢气(H2) 氯化锌、氯化钠
【解析】
(1)甲试管中,锌与盐酸反应生成氯化锌和氢气,发生反应的化学方程式为:Zn+2HCl═ZnCl2+H2↑;
(2)四支试管,其中丁试管中的固体一定全部溶解,这是因为稀盐酸过量。故选丁。
(3)实验后将甲、乙、丙试管中的所有物质都倒入一个空烧杯中,稍后将丁试管中的物质倒入此烧杯中,有气泡产生,是因为稀盐酸和过量的锌反应生成了氢气,此气泡的气体物质是氢气,静置后,烧杯内上部的澄清液中的溶质一定含有碳酸钠和稀盐酸反应生成的氯化钠、锌和稀盐酸、氯化铜反应生成的氯化锌。

练习册系列答案
 中考解读考点精练系列答案
中考解读考点精练系列答案
相关题目