题目内容
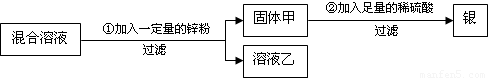
(2011?宜昌)小明和小丽对蓝色的硫酸铜溶液很感兴趣,他们设计如下实验探究其相关性质并对反应后所得物质进行分析和处理.
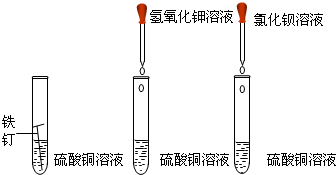
(1)我能写出其中两个不同基本反应类型的化学方程式:①
(2)实验完毕,小明和小丽各自将三个反应所得到的物质混合、过滤,得到甲、乙两种无色溶液.小明取少量甲溶液于试管中,滴加紫色石蕊溶液,试管中溶液呈紫色.则甲溶液中一定含有的溶质是
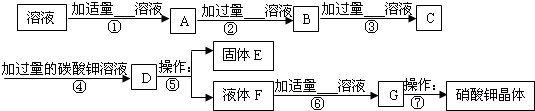
在步骤⑦中进行的操作是

(1)我能写出其中两个不同基本反应类型的化学方程式:①
Fe+CuSO4=FeSO4+Cu
Fe+CuSO4=FeSO4+Cu
;②CuSO4+2KOH=K2SO4+Cu(OH)2↓
CuSO4+2KOH=K2SO4+Cu(OH)2↓
.(2)实验完毕,小明和小丽各自将三个反应所得到的物质混合、过滤,得到甲、乙两种无色溶液.小明取少量甲溶液于试管中,滴加紫色石蕊溶液,试管中溶液呈紫色.则甲溶液中一定含有的溶质是
KCl
KCl
(填化学式,下同),可能含有的溶质是K2SO4
K2SO4
或BaCl2
BaCl2
.小丽对乙溶液进行了探究,发现乙溶液中含有氯化钾、硫酸钾和氢氧化钾.她说:我能设计如下实验,在步骤①、②、③中每次用一种无色溶液除去乙溶液中一种物质,且每步均有白色沉淀生成,最后得到纯净的硝酸钾晶体.
在步骤⑦中进行的操作是
蒸发
蒸发
,步骤③、⑥所加物质分别是AgNO3
AgNO3
、HNO3
HNO3
(填化学式,下同),固体E的成分有Mg(OH)2、BaSO4、AgCl、Ag2CO3、BaCO3
Mg(OH)2、BaSO4、AgCl、Ag2CO3、BaCO3
.分析:(1)根据图示中反应中所使用的试剂,判断每个图所发生的反应并对反应进行分类,然后写出两个不同反应类型的反应的化学方程式;
(2)分析三个反应后所得溶液混合后可能发生的反应,结合混合后所得甲溶液为无色且呈中性的特点,推断溶液的组成;
根据乙溶液中含有的氯化钾、硫酸钾和氢氧化钾的性质,分析向该溶液中每次用一种无色溶液除去乙溶液中一种物质且每步均有白色沉淀生成的设计要求,判断在步骤①、②、③中所使用的试剂及反应后形成的沉淀及所得溶液,结合最后得到纯净的硝酸钾晶体的实验目的,完成对固体E的推断及操作⑥所使用的试剂.
(2)分析三个反应后所得溶液混合后可能发生的反应,结合混合后所得甲溶液为无色且呈中性的特点,推断溶液的组成;
根据乙溶液中含有的氯化钾、硫酸钾和氢氧化钾的性质,分析向该溶液中每次用一种无色溶液除去乙溶液中一种物质且每步均有白色沉淀生成的设计要求,判断在步骤①、②、③中所使用的试剂及反应后形成的沉淀及所得溶液,结合最后得到纯净的硝酸钾晶体的实验目的,完成对固体E的推断及操作⑥所使用的试剂.
解答:解:(1)铁与硫酸铜发生置换反应生成硫酸亚铁和铜,反应的化学方程式为Fe+CuSO4=FeSO4+Cu;硫酸铜与滴加的氢氧化钾发生复分解反应,通过交换成分生成硫酸钾和氢氧化铜沉淀,反应的化学方程式为CuSO4+2KOH=K2SO4+Cu(OH)2↓;硫酸铜与滴加的氯化钡发生复分解反应,通过交换成分生成硫酸钡沉淀和氯化铜,反应的化学方程式为BaCl2+CuSO4=BaSO4↓+CuCl2;三个反应可分类置换反应和复分解反应两种反应类型;
(2)铁与硫酸铜反应后的溶液中一定含有硫酸亚铁,氢氧化钾与硫酸铜反应后的溶液中一定含有硫酸钾,氯化钡与硫酸铜反应后的溶液中一定含有氯化铜.三个反应所得到的物质混合后得到无色溶液,而含亚铁离子或铜离子的溶液分别呈绿色或蓝色,因此可判断三个反应所得到的物质混合时,溶液中亚铁离子、铜离子全部反应而沉淀,则所加过量氢氧化钾溶液使这两种离子形成沉淀同时生成硫酸钾和氯化钾;由于紫色石蕊仍呈紫色,说明三者混合后溶液呈中性,可判断氢氧化钾应与溶液中亚铁离子、铜离子恰好完全反应.再考虑到由于硫酸钾会与可能过量的氯化钡反应生成硫酸钡沉淀和氯化钾;因此,甲溶液中一定含有氯化钾,可能含有硫酸钾或氯化钡;
步骤⑦的操作完成后,由溶液得到晶体,因此可判断此时的操作应为蒸发,通过蒸发溶液而获得晶体;
为逐步进行沉淀乙溶液中含有氯化钾、硫酸钾和氢氧化钾,步骤①可加入适量的硝酸镁与氢氧化钾反应生成氢氧化镁沉淀和硝酸钾,然后在步骤②加入过量硝酸钡与硫酸钾反应生成硫酸钡沉淀和硝酸钾,在步骤③中过量硝酸银使溶液中氯离子全部沉淀而得到硝酸盐的溶液;接下来的步骤④通过加入过量碳酸钾使溶液中的镁离子、钡离子、银离子全部沉淀,至此所得溶液为硝酸钾与碳酸钾的混合溶液,步骤⑤过滤除去沉淀后再经过步骤⑥加入适量稀硝酸则可溶液变为硝酸钾溶液,蒸发后得到硝酸钾晶体;步骤⑤得到的固体E为前四步所形成的沉淀,因此该固体可能含有氢氧化镁沉淀、硫酸钡沉淀、氯化银沉淀、碳酸钡沉淀、碳酸银沉淀等.
故答案为:
(1)Fe+CuSO4=FeSO4+Cu;CuSO4+2KOH=K2SO4+Cu(OH)2↓ (或BaCl2+CuSO4=BaSO4↓+CuCl2)
(2)KCl;K2SO4;BaCl2;
蒸发;AgNO3;HNO3;Mg(OH)2、BaSO4、AgCl、Ag2CO3、BaCO3[或BaSO4、AgCl、Ag2CO3、Zn(OH)2、ZnCO3或BaSO4、AgCl、Ag2CO3、Zn(OH)2、BaCO3].
(2)铁与硫酸铜反应后的溶液中一定含有硫酸亚铁,氢氧化钾与硫酸铜反应后的溶液中一定含有硫酸钾,氯化钡与硫酸铜反应后的溶液中一定含有氯化铜.三个反应所得到的物质混合后得到无色溶液,而含亚铁离子或铜离子的溶液分别呈绿色或蓝色,因此可判断三个反应所得到的物质混合时,溶液中亚铁离子、铜离子全部反应而沉淀,则所加过量氢氧化钾溶液使这两种离子形成沉淀同时生成硫酸钾和氯化钾;由于紫色石蕊仍呈紫色,说明三者混合后溶液呈中性,可判断氢氧化钾应与溶液中亚铁离子、铜离子恰好完全反应.再考虑到由于硫酸钾会与可能过量的氯化钡反应生成硫酸钡沉淀和氯化钾;因此,甲溶液中一定含有氯化钾,可能含有硫酸钾或氯化钡;
步骤⑦的操作完成后,由溶液得到晶体,因此可判断此时的操作应为蒸发,通过蒸发溶液而获得晶体;
为逐步进行沉淀乙溶液中含有氯化钾、硫酸钾和氢氧化钾,步骤①可加入适量的硝酸镁与氢氧化钾反应生成氢氧化镁沉淀和硝酸钾,然后在步骤②加入过量硝酸钡与硫酸钾反应生成硫酸钡沉淀和硝酸钾,在步骤③中过量硝酸银使溶液中氯离子全部沉淀而得到硝酸盐的溶液;接下来的步骤④通过加入过量碳酸钾使溶液中的镁离子、钡离子、银离子全部沉淀,至此所得溶液为硝酸钾与碳酸钾的混合溶液,步骤⑤过滤除去沉淀后再经过步骤⑥加入适量稀硝酸则可溶液变为硝酸钾溶液,蒸发后得到硝酸钾晶体;步骤⑤得到的固体E为前四步所形成的沉淀,因此该固体可能含有氢氧化镁沉淀、硫酸钡沉淀、氯化银沉淀、碳酸钡沉淀、碳酸银沉淀等.
故答案为:
(1)Fe+CuSO4=FeSO4+Cu;CuSO4+2KOH=K2SO4+Cu(OH)2↓ (或BaCl2+CuSO4=BaSO4↓+CuCl2)
(2)KCl;K2SO4;BaCl2;
蒸发;AgNO3;HNO3;Mg(OH)2、BaSO4、AgCl、Ag2CO3、BaCO3[或BaSO4、AgCl、Ag2CO3、Zn(OH)2、ZnCO3或BaSO4、AgCl、Ag2CO3、Zn(OH)2、BaCO3].
点评:本题涉及的物质繁杂,熟练掌握酸、碱、盐类物质的通性是解答此问题的基础,进行合理分析则是解答本题的关键和难点.

练习册系列答案
相关题目
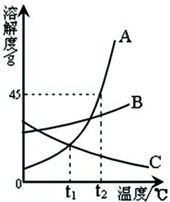 (2011?宜昌)右图是A、B、C三种物质的溶解度曲线,我能根据此图回答下列问题:
(2011?宜昌)右图是A、B、C三种物质的溶解度曲线,我能根据此图回答下列问题: