题目内容
【题目】为比较相同浓度的FeCl3溶液和CuSO4溶液对H2O2分解的催化效果,某研究小组进行了如下探究:
(1)请写出H2O2分解的化学方程式_____________________________.
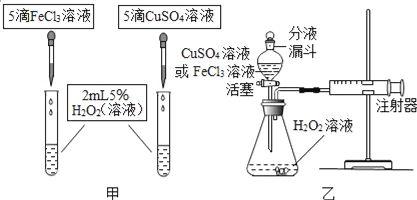
【定性研究】(2)如图甲,可通过观察___________来定性比较两者的催化效果.
【定量研究】(3)如图乙,要定量比较两者的催化效果,可测量生成等体积气体所需的______.
【深入研究】(4)在FeCl3溶液中,究竟是哪种粒子起催化作用呢?猜想1:铁离子(Fe3+)起催化作用; 猜想2:__起催化作用;猜想3:__起催化作用。
【答案】 2H2O2![]() 2H2O+O2↑ 产生气泡的速率 时间 氯离子(或Cl-) 水分子(或H2O)
2H2O+O2↑ 产生气泡的速率 时间 氯离子(或Cl-) 水分子(或H2O)
【解析】(1)过氧化氢在催化剂的作用下分解为氧气和水,故填:2H2O2![]() 2H2O+O2↑;
2H2O+O2↑;
(2)比较两种物质对过氧化氢分解速率的影响,可以观察二者产生气泡的速率;故填:产生气泡的速率;
(3)催化剂的催化效果越好,反应产生气体的速率越快,可通过测量产生等体积的氧气所需要的时间来分析,所需时间越短,催化效果越好;
(4)氯化铁溶液中存在铁离子、氯离子和水分子,故猜想可能是铁离子或氯离子或水分子所起的催化作用。

 探究与巩固河南科学技术出版社系列答案
探究与巩固河南科学技术出版社系列答案【题目】学习了MnO2对过氧化氢分解有催化作用的知识后,某同学想:CuO能否起到类似MnO2的催化剂作用呢?于是进行了以下探究。
【猜想】Ⅰ、CuO不是催化剂、也不参与反应,反应前后质量和化学性质不变;
Ⅱ、CuO参与反应产生O2,反应前后质量和化学性质发生了改变;
Ⅲ、CuO是反应的催化剂,反应前后_____________________________。
【实验】用天平称量0.2gCuO,取5mL5%的过氧化氢溶液于试管中,进行如下实验:
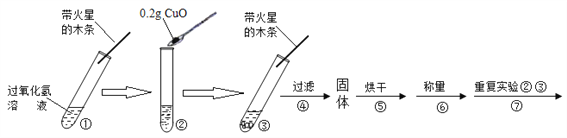
(1)填写下表:
步骤③现象 | 步骤⑥结果 | 步骤⑦现象 | 结论 |
________ 带火星的木条复燃。 | ______ | 溶液中有气泡放出,________ | 猜想Ⅰ、Ⅱ不成立; 猜想Ⅲ成立。 |
(2)步骤①的目的是___________________________________。
(3)步骤④需用到的实验仪器有:铁架台(带铁圈)、漏斗、烧杯、___________。
(4)过氧化氢能被CuO催化分解的化学方程式为_______________________。
【拓展】要探究步骤⑤做过催化剂的CuO其它化学性质,还应补做的实验是____。(写一种)
【题目】铁及其化合物有广泛的应用.
(一)铁的广泛应用
(1)“加铁酱油”中的铁指的是________(填字母).
A. 单质 B.元素 C.原子
(2)铁制炊具加热食物,说明铁具有的性质是_______.
(3)铁与铬、镍等金属熔合可形成“不锈钢”,用不锈钢丝和聚乙烯纤维为原料可制作耐酸防护服材料.以上叙述中不涉及到_______(填字母).
A.合金 B.无机非金属材料 C.合成材料 D.复合材料
(二)草酸亚铁晶体组成的测定
草酸亚铁晶体(化学组成为FeC2O4·xH2O)是一种淡黄色晶体粉末.
【查阅资料】Ⅰ. CO能与氯化钯(PdCl2)溶液反应生成黑色的钯粉;
Ⅱ. FeO和Fe3O4都是黑色物质,FeO在空气中不稳定,易被氧化.
草酸亚铁晶体受热分解生成四种氧化物,为确定分解产物及x的值,设计了如下实验进行探究:(装置C、D、E中药品均足量)
【实验设计】
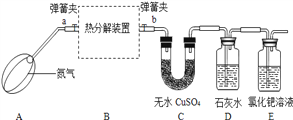
【实验步骤】
(1)连接装置,___________;
(2)称装置B中固体质量、装置C的质量;
(3)在装置B中装入一定质量的草酸亚铁晶体,打开弹簧夹a、b,鼓入一段时间氮气;
(4)用酒精灯加热B装置,直至晶体完全变成黑色,停止加热;
(5)继续通氮气至装置冷却,关闭弹簧夹a、b;
(6)再次称量装置B中固体质量、装置C的质量.
【进行实验】该小组同学按上述实验步骤进行实验,并记录了如下数据:
装置B中固体质量(/g) | 装置C的质量(/g) | |
实验前 | 9.0 | 168.2 |
实验后 | 3.6 | 170.0 |
【实验分析及数据处理】
(1)加热前先鼓入一段时间氮气的目的是_______;
(2)实验过程中,装置C中固体变为蓝色,说明草酸亚铁晶体分解生成了________,FeC2O4·xH2O中x的值为____;实验结束后若不继续通氮气,X值____(填“偏大”、“不变”或“偏小”);
(3)装置D中石灰水变浑浊,说明草酸亚铁晶体分解生成了______;
(4)装置E出现黑色物质,说明草酸亚铁晶体分解生成了______;同时装置E还具有的作用是______;
(5)根据上表数据,计算反应后装置B中残留黑色物质的化学式______;
(6)实验后,装置B中固体的颜色由淡黄色变成黑色,
写出草酸亚铁晶体受热分解的化学方程式: ___;
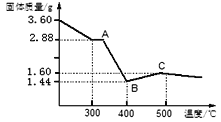
【定量研究】
取3.60g草酸亚铁晶体在坩埚中敞口充分加热,固体质量随温度变化的曲线如下图所示,写出BC段发生反应的化学方程式:________.
【题目】鉴别下列各组物质的方法不正确的是
选项 | 鉴别的物质 | 鉴别的方法 |
A | 纯水和矿泉水 | 观察是否澄清 |
B | 二氧化碳和一氧化碳 | 点燃,观察是否能燃烧 |
C | 水和过氧化氢溶液 | 加二氧化锰,观察是否有气泡 |
D | 冰和干冰 | 室温(20℃)放置,过一段时间观察是否有液体残留 |
A. A B. B C. C D. D