题目内容
(2008?大连)高锰酸钾中氧元素的质量分数与氯酸钾中氧元素的质量分数相差很小,但等质量的高锰酸钾和氯酸钾(另加少量二氧化锰作催化剂)分别加热,充分反应后,高锰酸钾分解产生的氧气的质量却远远小于氯酸钾分解产生的氧气的质量.运用所学知识解释原因.
分析:根据质量守恒定律,氧元素反应前后守恒,追寻反应前后氧元素是否全部转化为氧气是解题的关键.
解答:解:解:高锰酸钾加热制氧气的化学方程式为 2KMnO4
K2MnO4+MnO2+O2↑;
加热氯酸钾与二氧化锰制氧气的化学方程式为2KClO3
2KCl+3O2↑;
由上述化学方程式不难看出:高锰酸钾中的氧元素只有部分转化为氧气单质,氯酸钾中的氧元素全部转化为氧气.故等质量的高锰酸钾和氯酸钾分别加热,充分反应后,高锰酸钾分解产生氧气的质量却远远小于氯酸钾分解产生氧气的质量.
故答为:高锰酸钾完全分解生成K2MnO4和MnO2中含有一部分氧元素,所以高锰酸钾中的氧元素并没有完全转化成氧气;而氯酸钾分解生成的KCl中不含氧元素,可见氯酸钾中的氧元素完全转化为氧气了.所以等质量的氯酸钾比高锰酸钾放出的氧气多.
| ||
加热氯酸钾与二氧化锰制氧气的化学方程式为2KClO3
| ||||
| △ |
由上述化学方程式不难看出:高锰酸钾中的氧元素只有部分转化为氧气单质,氯酸钾中的氧元素全部转化为氧气.故等质量的高锰酸钾和氯酸钾分别加热,充分反应后,高锰酸钾分解产生氧气的质量却远远小于氯酸钾分解产生氧气的质量.
故答为:高锰酸钾完全分解生成K2MnO4和MnO2中含有一部分氧元素,所以高锰酸钾中的氧元素并没有完全转化成氧气;而氯酸钾分解生成的KCl中不含氧元素,可见氯酸钾中的氧元素完全转化为氧气了.所以等质量的氯酸钾比高锰酸钾放出的氧气多.
点评:该题出的很巧妙,以制取氧气的原理及元素守恒入手,从量的方面考查两种制取氧气的方法.

练习册系列答案
相关题目
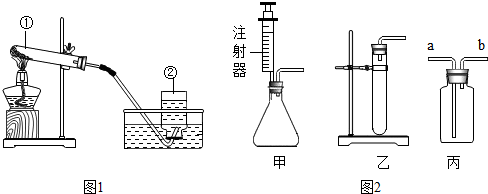
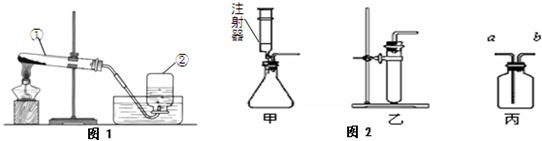
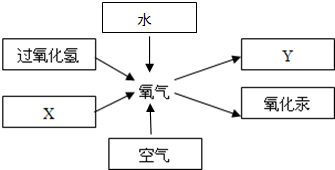
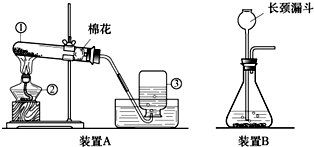 实验室常用制取氧气的方法有:
实验室常用制取氧气的方法有: