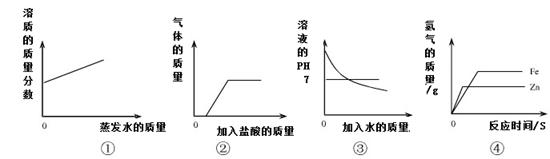
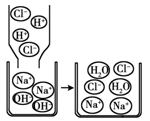
��Ŀ����
��7�֣���ҵ�Ͽ�����ʳ�κ�ʯ��ʯΪԭ����ȡ���Na2CO3���������Ĺؼ����ڳ���������NaCl��NH3��CO2��H2O�����ܶ��ת����NaHCO3������������NH4Cl����Һ������Ҫ�����������£�����֪2NH4Cl+Ca(OH)2=CaCl2+2NH3 ��+2H2O��
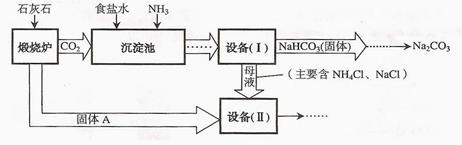
��1��������¯���з�����Ӧ�Ļ�ѧ����ʽ�� ��
��2�����ڻ�ѧʵ��������롰�豸��I�����еĻ����õ��IJ��������� ���ò������õ��IJ����������ձ��� �� ��
��3���ڡ��豸�����й���A��ˮ��Ӧ�Ļ�ѧ����ʽ�� ��
��4���ԡ��豸�����е�ĸҺ������ˮ������ڱ������������õ������� ����д��ѧʽ����
��5����д�����Na2CO3����һ����;��

��1��������¯���з�����Ӧ�Ļ�ѧ����ʽ�� ��
��2�����ڻ�ѧʵ��������롰�豸��I�����еĻ����õ��IJ��������� ���ò������õ��IJ����������ձ��� �� ��
��3���ڡ��豸�����й���A��ˮ��Ӧ�Ļ�ѧ����ʽ�� ��
��4���ԡ��豸�����е�ĸҺ������ˮ������ڱ������������õ������� ����д��ѧʽ����
��5����д�����Na2CO3����һ����;��
��CaCO3 CaO+CO2�� �ƹ��� ©�� ������ ��H2O+CaO===Ca(OH)2
CaO+CO2�� �ƹ��� ©�� ������ ��H2O+CaO===Ca(OH)2
��NH3��NaCl�����1�������֣� �����ڲ�������ֽ����֯��ϴ�Ӽ���������
 CaO+CO2�� �ƹ��� ©�� ������ ��H2O+CaO===Ca(OH)2
CaO+CO2�� �ƹ��� ©�� ������ ��H2O+CaO===Ca(OH)2 ��NH3��NaCl�����1�������֣� �����ڲ�������ֽ����֯��ϴ�Ӽ���������
(1)������¯��������ʯ��ʯ��CaCO3 CaO+CO2������2����������Һ�����Ļ�������Ϊ���ˣ������õ��IJ����������ձ��⣬����©���Ͳ���������3��������ʯ��ʯ��CaCO3
CaO+CO2������2����������Һ�����Ļ�������Ϊ���ˣ������õ��IJ����������ձ��⣬����©���Ͳ���������3��������ʯ��ʯ��CaCO3 CaO+CO2����֪����AΪCaO����ˮ��Ӧ�Ļ�ѧ����ʽΪCaO +H2O ==Ca(OH)2����4���ڡ��豸������2NH4Cl+Ca(OH)2==CaCl2+H2O+NH3�������ɳ������Ϸ�����ʳ��ˮ��NH3����֪�����õ�������NaCl��NH3����5�����Na2CO3���Ŀ����ڲ�������ֽ����֯��ϴ�Ӽ��������ȣ������г���������ͷ��
CaO+CO2����֪����AΪCaO����ˮ��Ӧ�Ļ�ѧ����ʽΪCaO +H2O ==Ca(OH)2����4���ڡ��豸������2NH4Cl+Ca(OH)2==CaCl2+H2O+NH3�������ɳ������Ϸ�����ʳ��ˮ��NH3����֪�����õ�������NaCl��NH3����5�����Na2CO3���Ŀ����ڲ�������ֽ����֯��ϴ�Ӽ��������ȣ������г���������ͷ��
 CaO+CO2������2����������Һ�����Ļ�������Ϊ���ˣ������õ��IJ����������ձ��⣬����©���Ͳ���������3��������ʯ��ʯ��CaCO3
CaO+CO2������2����������Һ�����Ļ�������Ϊ���ˣ������õ��IJ����������ձ��⣬����©���Ͳ���������3��������ʯ��ʯ��CaCO3 CaO+CO2����֪����AΪCaO����ˮ��Ӧ�Ļ�ѧ����ʽΪCaO +H2O ==Ca(OH)2����4���ڡ��豸������2NH4Cl+Ca(OH)2==CaCl2+H2O+NH3�������ɳ������Ϸ�����ʳ��ˮ��NH3����֪�����õ�������NaCl��NH3����5�����Na2CO3���Ŀ����ڲ�������ֽ����֯��ϴ�Ӽ��������ȣ������г���������ͷ��
CaO+CO2����֪����AΪCaO����ˮ��Ӧ�Ļ�ѧ����ʽΪCaO +H2O ==Ca(OH)2����4���ڡ��豸������2NH4Cl+Ca(OH)2==CaCl2+H2O+NH3�������ɳ������Ϸ�����ʳ��ˮ��NH3����֪�����õ�������NaCl��NH3����5�����Na2CO3���Ŀ����ڲ�������ֽ����֯��ϴ�Ӽ��������ȣ������г���������ͷ��
��ϰ��ϵ�д�
�����Ŀ