题目内容
【题目】金属和金属材料在生产生活中应用广泛.
(1)下列铁制品的用途中,利用金属导热性的是______(填字母,下同).
A 铁锤 B 铁锅
B 铁锅 C 铁丝
C 铁丝 D 水龙头
D 水龙头
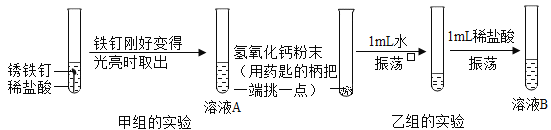
(2)除去生锈的铁制品表面的锈,可加入适量的稀盐酸,写出发生反应的化学方程式______.
(3)小明同学做了金属与盐溶液反应的实验探究,他向Zn(NO3)2、AgNO3、Cu(NO3)2的混合溶液中加入一定量铁粉,完全反应后过滤,取滤渣于试管中,加稀盐酸,有气体生成,则反应后所得滤液中的溶质是______。
【答案】B Fe2O3+6HCl=2FeCl3+3H2O Zn(NO3)2、Fe(NO3)2
【解析】
(1)铁锅是利用铁的导热性,故选B;
(2)铁锈的主要成分是氧化铁,氧化铁与盐酸反应生成氯化铁和水;
故答案为:6HCl+Fe2O3=2FeCl3+3H2O;
(3)混合溶液中,金属活动性强弱关系锌>铁>铜>银,则铁粉先与AgNO3反应,再与Cu(NO3)2反应,而Zn的活动性比Fe大,所以Zn(NO3)2不与Fe反应;充分反应后过滤,向滤渣中滴加稀硫酸有可燃性气体产生,说明铁粉未过量,则溶液中的AgNO3、Cu(NO3)2全部被置换,而铁和Zn(NO3)2溶液不反应,滤液中含有Fe(NO3)2和Zn(NO3)2。

 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案 名校联盟快乐课堂系列答案
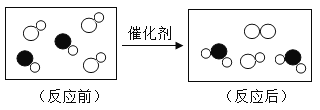
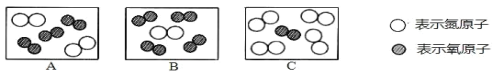
名校联盟快乐课堂系列答案【题目】某物质在点燃的条件下发生反应,生成物和反应物共四种,它们的微观示意图和反应前后的质量如下表所示。
物质序号 | 甲 | 乙 | 丙 | 丁 |
|
微观示意图 |
|
|
|
| |
反应前质量/g | 68 | 100 | 1 | 0 | |
反应后质量/g | 0 | x | y | z |
(1)表中的四种物质中,属于氧化物的是______ (填化学式);
(2)上述反应的化学方程式为______;
(3)一位同学在计算x、y和z数值的过程中,列出了以下等式,其中正确的是______(填字母序号)。
A x + y +z = 169 B y + z = 168 C (100-x):z = 32:64 D (l00-x):(y-1) = 8:3