题目内容
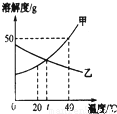
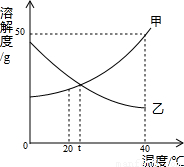
 请你用如图所示甲、乙两物质(均不含结晶水)的溶解度曲线解决以下问题.
请你用如图所示甲、乙两物质(均不含结晶水)的溶解度曲线解决以下问题.(1)40℃时50g水中加入30g甲物质,所得溶液的质量为
75
75
g.该温度下甲物质的饱和溶液中,溶质和溶液的质量比为1:3
1:3
.(2)分别将40℃时甲、乙的饱和溶液(无固体存在)降温至t℃,所得溶液中溶质的质量分数甲
>
>
乙(填“>”或“=”或“<”).(3)当甲中含有少量乙时,可以用
冷却热饱和溶液
冷却热饱和溶液
的方法提纯甲.分析:固体溶解度曲线所能表示的意义:①根据已知的温度可以查出有关物质的溶解度;②根据物质的溶解度也可以查出它所对应的温度;③可以判断或比较相同温度下,不同物质溶解度的大小(或饱和溶液中溶质的质量分数的大小);④根据溶解度曲线,选择分离、提纯某些可溶性混合物的方法(即选用蒸发结晶还是降温结晶);并且,还可以判断或比较析出晶体的质量大小,即曲线越陡,析出的晶体就越多;⑤两条溶解度曲线的交点表示该点所示的温度下,两物质的溶解度是相同的;并且,此时两种物质饱和溶液的溶质质量分数也相同的.
可以据此以上几点来完成解答.
可以据此以上几点来完成解答.
解答:解:(1)40℃时甲的溶解度为50g,即在该温度下100g水中最多能够溶解度50g甲物质,所以在40℃时50g水中加入30g甲物质,最多能够溶解25g甲物质,所得溶液的质量为50g+25g=75g.该温度下甲物质的饱和溶液中,溶质和溶液的质量比为50g:(100g+50g)=1:3.
(2)甲的溶解度随温度的升高而增大,所以若降低温度则甲会析出一部分溶质,而乙物质的溶解度随温度的升高而降低,所以若降低温度,乙的溶液的组成不变,即其溶质的质量分数不变,比较40℃时乙物质的溶解度和t℃时甲的溶解度可以知道40℃乙的溶解度依然小于t℃甲的溶解度,所以其溶质的质量分数小于甲的溶质的质量分数.
(3)甲的溶解度随温度的升高而增大,而乙物质的溶解度随温度的升高而降低,所以当甲中含有少量乙时,可以用冷却热饱和溶液的方法来提纯甲.
故答案为:(1)75;1:3;
(2)>;
(3)冷却热饱和溶液.
(2)甲的溶解度随温度的升高而增大,所以若降低温度则甲会析出一部分溶质,而乙物质的溶解度随温度的升高而降低,所以若降低温度,乙的溶液的组成不变,即其溶质的质量分数不变,比较40℃时乙物质的溶解度和t℃时甲的溶解度可以知道40℃乙的溶解度依然小于t℃甲的溶解度,所以其溶质的质量分数小于甲的溶质的质量分数.
(3)甲的溶解度随温度的升高而增大,而乙物质的溶解度随温度的升高而降低,所以当甲中含有少量乙时,可以用冷却热饱和溶液的方法来提纯甲.
故答案为:(1)75;1:3;
(2)>;
(3)冷却热饱和溶液.
点评:解答这类题目时,首先,要熟记和理解固体溶解度曲线及其使用,固体溶解度的概念和意义,溶质质量分数及其有关计算,饱和溶液和不饱和溶液的概念及其相互转变方法,以及物质的溶解和结晶的方法等相关知识;然后,根据所给的实验、问题情景或图表信息等,结合所学的相关知识和技能,细致地阅读、分析题意等最后,按照题目的要求,认真地进行选择或解答即可.

练习册系列答案
相关题目
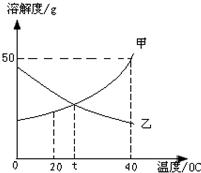 (2007?韶关)请你用如图所示甲、乙两物质(均不含结晶水)溶解度/g的溶解度曲线回答以下问题.
(2007?韶关)请你用如图所示甲、乙两物质(均不含结晶水)溶解度/g的溶解度曲线回答以下问题.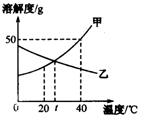 (2006?连云港)请你用如图所示甲、乙两物质(均不含结晶水)的溶解度曲线解决以下问题.
(2006?连云港)请你用如图所示甲、乙两物质(均不含结晶水)的溶解度曲线解决以下问题.