题目内容
【题目】我国的煤炭资源丰富,但液体燃料短缺。通过“煤液化”技术,用煤炭和水制取甲醇(CH3OH)对我国具有重要意义。主要流程如图:
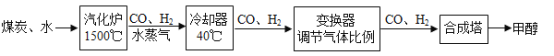
(1)投入汽化炉中的煤炭粉碎的目的是_____。
(2)汽化炉中发生的化学方程式是_____。
(3)为了提高原料的利用率,变换器中应控制合成气体积之比为:V(CO):V(H2)=_____。
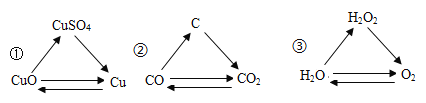
(4)利用CO、H2还可以合成多种物质。仅用CO、H2为原料不可能得到的物质是_____。
①乙醇(C2H6O) ②尿素(CO(NH2)2) ③甲醛(CH6O)
(5)“煤液化”相对于传统的“燃煤”的优点是_____。
【答案】增大反应的接触面积,使反应更充分  1:2 ①② 减少大气污染物的排放(或提高了能源的利用率)
1:2 ①② 减少大气污染物的排放(或提高了能源的利用率)
【解析】
(1)投入汽化炉中的煤炭粉碎的目的是增大反应的接触面积,使反应更充分。故填:增大反应的接触面积,使反应更充分;
(2)汽化炉中碳和水蒸气在高温条件下反应,生成一氧化碳和氢气,发生的化学方程式是: 。故填:
。故填: ;
;
(3)合成甲醇的方程式为CO+2H2→CH3OH,由方程式可知上述工艺中应控制合成气中V(CO):V(H2)=1:2,故填:1:2;
(4)由质量守恒定律可知化学反应前后元素的种类不变,可知反应前元素有三种即碳氢氧,反应后不会出现氮元素,所以尿素不可能产生;根据碳原子与氧原子个数比可知,①也不可能,故填:①②;
(5)“煤液化”相对于传统的“燃煤”的优点是减少大气污染物的排放(或提高了能源的利用率)。故填:减少大气污染物的排放(或提高了能源的利用率)。

练习册系列答案
 轻松课堂单元测试AB卷系列答案
轻松课堂单元测试AB卷系列答案 小题狂做系列答案
小题狂做系列答案
相关题目