题目内容
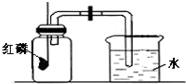 用来测定空气成分的方法很多,如图所示的是用红磷在空气中燃烧的测定方法.实验步骤如下:
用来测定空气成分的方法很多,如图所示的是用红磷在空气中燃烧的测定方法.实验步骤如下:
①在集气瓶按体积分为5等份,做好标记.
②检查装置的气密性.
③在燃烧匙内装入足量的红磷,将导管上的止水夹夹紧,在酒精灯上点燃红磷,立即伸入集气瓶中塞紧橡皮塞.
④充分反应后,待集气瓶冷却至室温,打开止水夹.
(1)写出步骤③化学反应的文字表达式为________.
(2)实验完毕,若进入集气瓶中水的体积不到总容积的1/5,你认为导致这一结果主要原因是什么:(写出两点即可)
①________;②________.
解:(1)磷和氧气在点燃的条件下生成五氧化二磷,故答案为:磷+氧气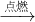 五氧化二磷
五氧化二磷
(2)本题中进入集气瓶中水的体积小于五分之一,有可能有以下几点:装置漏气、红磷的量不足、没有冷却就读数;故答案为:装置漏气、红磷的量不足或没有冷却就读数
分析:本题是用红磷测定空气中氧气的含量,本探究实验一般要注意以下几点:①装置的气密性好;②所用药品红磷的量,必须是足量;③读数时一定要冷却到原温度;④生成物的状态一般要求是固态等.如果控制不好条件,进入集气瓶中水体积会小于五分之一.如果装置内的部分空气逸散出来,就会导致进入集气瓶中水体积大于五分之一.
点评:本考点是用红磷测定氧气在空气中的体积分数,属于实验方法和过程的探究.这类探究实验要具体问题具体分析,根据设计的步骤中不同的现象去思考、去探究,从而回答题目给出的问题.本考点主要出现在填空题和实验题中.
 五氧化二磷
五氧化二磷(2)本题中进入集气瓶中水的体积小于五分之一,有可能有以下几点:装置漏气、红磷的量不足、没有冷却就读数;故答案为:装置漏气、红磷的量不足或没有冷却就读数
分析:本题是用红磷测定空气中氧气的含量,本探究实验一般要注意以下几点:①装置的气密性好;②所用药品红磷的量,必须是足量;③读数时一定要冷却到原温度;④生成物的状态一般要求是固态等.如果控制不好条件,进入集气瓶中水体积会小于五分之一.如果装置内的部分空气逸散出来,就会导致进入集气瓶中水体积大于五分之一.
点评:本考点是用红磷测定氧气在空气中的体积分数,属于实验方法和过程的探究.这类探究实验要具体问题具体分析,根据设计的步骤中不同的现象去思考、去探究,从而回答题目给出的问题.本考点主要出现在填空题和实验题中.

练习册系列答案
 课时训练江苏人民出版社系列答案
课时训练江苏人民出版社系列答案 黄冈经典趣味课堂系列答案
黄冈经典趣味课堂系列答案 启东小题作业本系列答案
启东小题作业本系列答案
相关题目
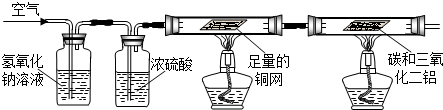
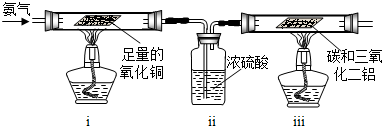
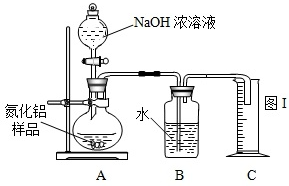

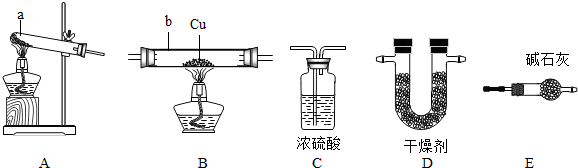
 NH3↑+CO2↑+H2O;②2NH3+H2SO4=(NH4)2SO4;③2NH3+3CuO
NH3↑+CO2↑+H2O;②2NH3+H2SO4=(NH4)2SO4;③2NH3+3CuO
