题目内容
 人类的生产生活离不开金属.(1)在地壳里含量居第二位的金属元素是
人类的生产生活离不开金属.(1)在地壳里含量居第二位的金属元素是铁
铁
.(2)下列三种金属被发现、使用的先后顺序依次为:铜、铁、铝.金属大规模被使用的先后顺序跟
C
C
(填字母)关系最大.A.地壳中金属元素的含量 B.金属的导电性 C.金属的活动性(3)某校化学兴趣小组同学利用金属进行了如下一些探究活动:
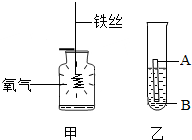
探究活动:在室温条件下进行如图所示实验(两装置的气密性都良好).已知:试管内的镁条和铁片表面均被打磨洁净,且形状、大小均相同;同时加入两支试管中的稀盐酸的质量和溶质质量分数均相等.
①该实验的目的是通过观察
比较镁、铁分别与盐酸反应放热速度
比较镁、铁分别与盐酸反应放热速度
而确定金属的活动性强弱
金属的活动性强弱
.两支长颈漏斗中产生的现象的不同之处是甲中长颈漏斗里的液面上升得更快
甲中长颈漏斗里的液面上升得更快
.②若实验所用的金属均过量,则充分反应后两装置产生的H2质量关系为
C
C
(填字母).A.甲多 B.乙多 C.一样多.
分析:(1)根据在地壳里元素的含量分析;
(2)根据金属制取的难易程度考虑;
(3)①根据金属的活动性分析;
②根据质量和溶质质量分数均相等的稀盐酸中含有的溶质的质量相同分析.
(2)根据金属制取的难易程度考虑;
(3)①根据金属的活动性分析;
②根据质量和溶质质量分数均相等的稀盐酸中含有的溶质的质量相同分析.
解答:解:(1)地壳中含量最多的前五种元素是氧、硅、铝、铁、钙,带金字旁的是金属,所以铝、铁、钙都是金属,第二位的是铁;
(2)金属越活泼的越不容易制取,所以与金属活动性有关.
(3))①如图2所示实验的目的是:通过比较镁、铁分别与盐酸反应放热速度来比较镁与铁的金属活动性强弱;因为镁反应快放热多,因此甲中长颈漏斗里的液面上升得更快.所以,该实验的目的是通过观察比较镁、铁分别与盐酸反应放热速度而确定金属的活动性强弱.两支长颈漏斗中产生的现象的不同之处是甲中长颈漏斗里的液面上升得更快.
②若实验所用的金属均过量,酸的质量相等,那么产生的氢气一样多.
故答案为:(1)铁;(2)C;(3)①比较镁、铁分别与盐酸反应放热速度,金属的活动性强弱;②C.
(2)金属越活泼的越不容易制取,所以与金属活动性有关.
(3))①如图2所示实验的目的是:通过比较镁、铁分别与盐酸反应放热速度来比较镁与铁的金属活动性强弱;因为镁反应快放热多,因此甲中长颈漏斗里的液面上升得更快.所以,该实验的目的是通过观察比较镁、铁分别与盐酸反应放热速度而确定金属的活动性强弱.两支长颈漏斗中产生的现象的不同之处是甲中长颈漏斗里的液面上升得更快.
②若实验所用的金属均过量,酸的质量相等,那么产生的氢气一样多.
故答案为:(1)铁;(2)C;(3)①比较镁、铁分别与盐酸反应放热速度,金属的活动性强弱;②C.
点评:本题的难度不是很大,主要考查了金属的活动性顺序的应用,从而培养了学生应用知识解决问题的能力.

练习册系列答案
 科学实验活动册系列答案
科学实验活动册系列答案
相关题目


 人类的生产生活离不开金属,下列三种金属被发现、使用的先后顺序依次为:铜、铁、铝.
人类的生产生活离不开金属,下列三种金属被发现、使用的先后顺序依次为:铜、铁、铝.