题目内容
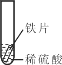
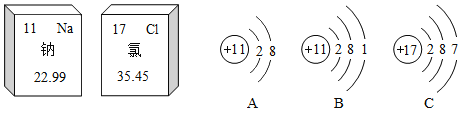
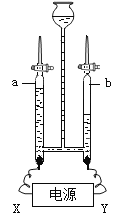
【题目】某老师在(燃烧的条件)教学中,改进了教材中的实验。如图所示,请回答:
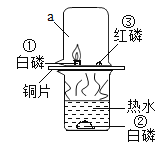
(1)对照①和③,能够获得可燃物燃烧需要的条件之一是____________。
(2)罩上仪器a的作用是____________。
(3)小明请教老师后获知:实验室中白磷保存在水中,其原因是_____________。
(4)白磷着火点是40℃,从室温低于40℃时白磷也会自燃的事实可以看出白磷在空气中缓慢氧化是_____________反应(填吸热或放热)
【答案】温度要达到可燃物的着火点 防止白磷燃烧产生的白烟进入空气,造成空气污染 使白磷与氧气隔绝,防止白磷自燃 放热
【解析】
本题考查的是对燃烧条件改进实验的探究分析。
(1)对照①和③,红磷和白磷同时放在温度相同的铜片上,且都与空气接触,白磷燃烧,而红磷不燃烧,说明可燃物燃烧需要的条件之一是温度要达到可燃物的着火点。
(2)罩上仪器a的作用是防止白磷燃烧产生的白烟进入空气,造成空气污染。
(3)根据燃烧的条件可知,可燃物要燃烧需要与氧气接触,因此,在实验室中把着火点较低的白磷保存在水中,目的是使白磷与氧气隔绝,防止白磷自燃。
(4)自燃是由于可燃物与氧气发生缓慢氧化放出热量,当热量不能扩散,温度达到了可燃物的着火点而自动燃烧的现象。白磷着火点是40℃,从室温低于40℃时,白磷与氧气发生缓慢氧化放出热量,当温度达到白磷的着火点时也会自燃。因此,白磷在空气中缓慢氧化是放热反应。

 海淀课时新作业金榜卷系列答案
海淀课时新作业金榜卷系列答案 期末金牌卷系列答案
期末金牌卷系列答案 轻松课堂标准练系列答案
轻松课堂标准练系列答案【题目】小聪同学家新换了水龙头,从说明书上了解到该水龙头是铜质镀铬。好奇的小聪想探究铬(Cr)与常见金属铁、铜的活动性强弱,邀请你一同参加。
(知识回放)
金属活动性顺序填写完整:K Ca Na Mg Al Zn______Sn Pb(H)______Hg Ag Pt Au
(作出猜想)
猜想1.Cr>Fe>Cu;猜想2. Fe>Cu >Cr;猜想3.你的猜想是_________。
(查阅资料)
(1)铬是银白色有光泽的金属,在空气中其表面能生成抗腐蚀的致密的氧化膜。
(2)铬能与稀硫酸反应,生成蓝色的硫酸亚铬(CrSO4)溶液。
(设计与实验)
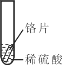
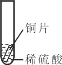
小聪同学取大小、形状相等的三种金属片,用砂纸打磨光亮;再取三支试管,分别放入等体积、等浓度的同种稀硫酸。
实验 | 试管1 | 试管2 | 试管3 |
实验 操作 |
|
|
|
实验 现象 | 铁片表面产生气泡较慢,溶液变为浅绿色 | 铬片表面产生气泡较快,溶液变成为蓝色 | _________ |
(结论与解释)
(1)小聪得到的结论是猜想_______正确。
(2)实验前用砂纸打磨金属片的目的是_____________。
(知识运用)
将铬片投入FeSO4溶液中,反应__________(填“能”或“不能”)进行。若能进行,请你写出反应的化学方程式_____________。
【题目】下面是小婷同学测定黄铜(铜锌合金)中铜的质量分数的过程。小婷同学取10 g黄铜于烧杯中,将120 g稀硫酸分六次加入烧杯中,测得加入的稀硫酸质量和烧杯中剩余物的质量如下表:
次数 | 一 | 二 | 三 | 四 | 五 | 六 |
加入稀硫酸的质量/g | 20 | 20 | 20 | 20 | 20 | 20 |
烧杯中剩余物的质量/g | 29.96 | 49.92 | m | 89.84 | 109.8 | 129.8 |
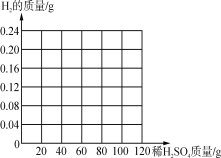
①10g黄铜完全反应产生H2的质量________g;
②表中m=________;
③求黄铜中铜的质量分数________ (写出计算过程)。
④请在如图画出10g黄铜加入稀硫酸与生成氢气的质量的图象________。