题目内容
【题目】草木灰可作肥料,同学取一些草木灰做了以下实验,请完成实验报告。
实验序号 | 实验目的 | 实验方案 | 实验现象 | 结论 | |
实验1 | 证明草木灰的主要成分含钾元素 | 取样,进行_________反应 | 透过蓝色钴玻璃片火焰呈__________色 | 草木灰主要成分含钾元素 | |
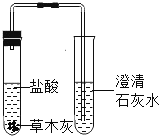
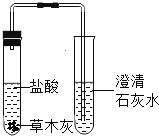
实验2 | _________ |
| _________ | 草木灰主要成分是碳酸钾 | |
实验3 | 探究碳酸钾性质 | 取样,向碳酸钾溶液中滴入石灰水溶液 | 生成白色沉淀 | 写反应化学方程式__________ | |
分析推测:实验3反应后上层清液中溶质成分组成____________________________ | |||||
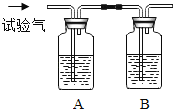
实验4 | 探究实验3反应后上层清液中溶质成分 | 对实验3反应后的上层清液进行一次取样。 _________ | _________ | 反应后上层清液溶质成分是只含氢氧化钾 | |
【答案】焰色 紫色 证明草木灰的主要成分是K2CO3 有气泡产生,澄清石灰水变浑浊 K2CO3+Ca(OH) 2=2KOH+CaCO3↓ ①KOH ②KOH、 K2CO3 ③KOH 、 Ca(OH) 2 滴加足量稀盐酸,再滴加足量Na2CO3溶液 无气泡产生,无沉淀产生(无明显现象)
【解析】
实验1 钾元素的焰色反应是透过蓝色钴玻璃片火焰呈紫色;
实验2 碳酸盐和酸反应会生成二氧化碳,二氧化碳能使澄清石灰水变浑浊;
实验3 碳酸钾和氢氧化钙反应生成碳酸钙沉淀和氢氧化钾;
碳酸钾和氢氧化钙可能恰好完全反应,也可能其中的一种物质过量;
实验4酸会与碳酸根离子生成二氧化碳气体,碳酸根离子和钙离子会生成碳酸钙沉淀沉淀,所以
实验序号 | 实验目的 | 实验方案 | 实验现象 | 结论 |
| 证明草木灰的主要成分含钾元素 | 取样,进行焰色反应 | 透过蓝色钴玻璃片火焰呈紫色 | 草木灰主要成分含钾元素 |
| 证明草木灰主要成分是碳酸钾 |
|
|
|
实验3 | 探究碳酸钾性质 | 取样,向碳酸钾溶液中滴入石灰水溶液 | 生成白色沉淀 | 化学方程式为: |
分析推测:实验3反应后上层清液中溶质成分组成①KOH②KOH、K2CO3③KOH、Ca(OH)2 | ||||
实验4 | 探究实验3反应后上层清液中溶质成分 | 对实验3反应后的上层清液进行一次取样. | 无气泡产生,无沉淀产生(无明显现象) | 反应后上层清液溶质成分是只含氢氧化钾 |

【题目】下表是NaCl、KNO3在不同温度时的溶解度,根据数据回答。
温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | |
溶解度 | NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 |
(g/100g水) | KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 |
①氯化钠的溶解度受温度变化的影响_____(填“很大”或“很小”)。
②50℃时,KNO3的溶解度_____(填“<”、“>”或“=”)NaCl的溶解度;向烧杯中加入100g水和49.0gKNO3固体配成50℃的溶液,再冷却到20℃,烧杯中析出固体的质量为_____g。
③KNO3中混有少量的NaCl,提纯的方法是_____(填“降温结晶”或“蒸发结晶”)。
④要比较NaCl和KNO3在水中的溶解性强弱,测定的数据可以是:相同温度下,等质量的溶质完全溶解达到饱和时所需水的质量;或_____。
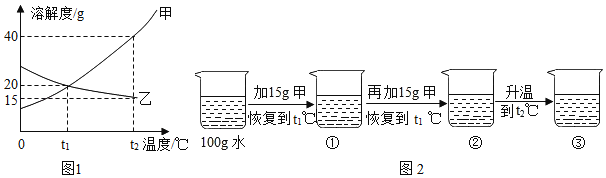
⑤如图是有关硝酸钾溶液的实验操作及变化情况,说法正确的是_____(填编号)。
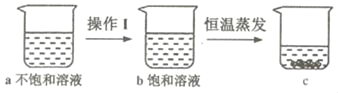
A 操作I一定是降温
B a与b的溶剂质量可能相等
C a与c的溶质质量一定相等
D b与c的溶质质量分数一定相等