题目内容
【题目】A~F是初中化学所学的常见物质,其转化关系如图所示(部分反应物和生成物、反应条件已略去)。B是白色难溶固体,其中相对分子质量为100,C俗称纯碱,F是最常见溶剂。
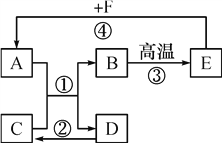
请回答:A的一种用途是____________;反应①和③的化学方程式分别为______________________、______________________;反应④发生时的一个明显现象是__________________。
【答案】 改良酸性土壤 Ca(OH)2+Na2CO3===CaCO3↓+2NaOH CaCO3![]() CaO+CO2↑ 固体溶解,放出热量
CaO+CO2↑ 固体溶解,放出热量
【解析】B是白色难溶固体,其中相对分子质量为100故B为碳酸钙,C俗称纯碱C为碳酸钠,F是最常见溶剂,F是水,碳酸钙高温分解生成氧化钙和二氧化碳,反应方程式为:CaCO3![]() CaO+CO2↑,氧化钙和水生成氢氧化钙,氢氧化钙和碳酸钠反应生成碳酸钙和水,反应方程式为:Ca(OH)2+Na2CO3===CaCO3↓+2NaOH。所以A是氢氧化钙,氢氧化钙的用途有:改良酸性土壤;氧化钙和水反应的现象是:固体逐渐溶解,放出大量热。
CaO+CO2↑,氧化钙和水生成氢氧化钙,氢氧化钙和碳酸钠反应生成碳酸钙和水,反应方程式为:Ca(OH)2+Na2CO3===CaCO3↓+2NaOH。所以A是氢氧化钙,氢氧化钙的用途有:改良酸性土壤;氧化钙和水反应的现象是:固体逐渐溶解,放出大量热。

 阅读快车系列答案
阅读快车系列答案【题目】同学们在学习碱的化学性质时,进行了如图所示的实验: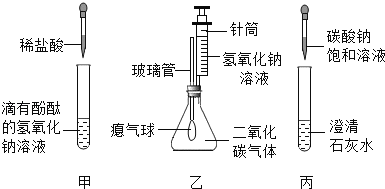
(1)乙实验中滴加氢氧化钠溶液后,可观察到的现象是 ,发生反应的化学方程式为 .
(2)丙实验中观察到的实验现象是 .
(3)实验结束后,同学们将甲、乙、丙三个实验的废液倒入同一个干净的废液缸中,最终看到废液浑浊并呈红色,产生疑问.
【提出问题】废液中含有哪些物质?
【交流讨论】
①一定含有的物质:指示剂、水、硫酸钠、碳酸钙.
②还含有能使废液呈碱性的物质,能使废液呈碱性的物质是什么?
同学们有如下猜想:
小丽认为:有氢氧化钠和碳酸钠
小明认为:只有碳酸钠
小平认为:只有氢氧化钠
你认为可能的是 (写一种猜想).
【实验设计】小芳想用氯化钙溶液来验证以上三个同学的猜想,通过查阅资料获悉氯化钙溶液呈中性,并设计如下实验,请你将小芳的实验设计补充完整.
实验内容 | 预计现象 | 预计结论 |
取少量废液缸中上层清液于试管中,加入过量氯化钙溶液,静置 | ①有白色溶液,溶液呈红色 | 小丽的猜想正确 |
② | 小明的猜想正确 | |
③ | 小平的猜想正确 |