题目内容
【题目】为测定某化工厂废水中硫酸的溶质质量分数。同学们做了如下实验(废水中的其他成分不与铁发生反应)。
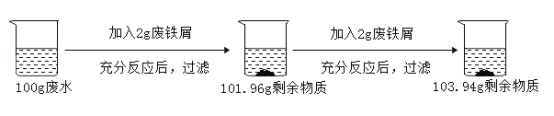
(1)反应共生成氢气____________g。
(2)废水中硫酸的溶质质量分数是多少?______
【答案】0.06 2.94%
【解析】
(1)反应物的总质量为![]() ,反应后烧杯内物质的总质量为103.94g,根据.质量守恒定律,烧杯中减少的质量就是生成氢气的质量,所以氢气的质量为
,反应后烧杯内物质的总质量为103.94g,根据.质量守恒定律,烧杯中减少的质量就是生成氢气的质量,所以氢气的质量为![]() 。
。
(2)第一次加入2g废铁屑,生成氢气质量为![]() ;第二次加入2g废铁屑,生成氢气的质量为
;第二次加入2g废铁屑,生成氢气的质量为![]() ,说明100g稀硫酸已反应完,第二次加入的2g废铁屑没有反应完,应根据生成氢气的总质量计算稀硫酸中溶质的质量,进而计算废水中硫酸的溶质质量分数。
,说明100g稀硫酸已反应完,第二次加入的2g废铁屑没有反应完,应根据生成氢气的总质量计算稀硫酸中溶质的质量,进而计算废水中硫酸的溶质质量分数。
解:设废水中硫酸溶质的质量为x
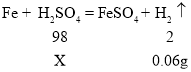
![]()
x=2.94g
废水中硫酸的溶质质量分数为![]()
答:废水中硫酸的溶质质量分数为2.94%。

练习册系列答案
 导学与测试系列答案
导学与测试系列答案 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案
相关题目