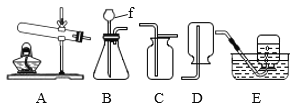题目内容
【题目】过氧乙酸对细菌和病毒具有高效、快速杀灭作用,广泛应用于环境的消毒,如图为过氧乙酸的分子结构图(其中![]() 代表碳原子,
代表碳原子,![]() 代表氢原子,
代表氢原子,![]() 代表氧原子),下列有关说法正确的是( )
代表氧原子),下列有关说法正确的是( )
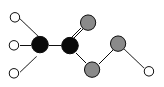
A. 过氧乙酸的化学式是CH3COOOH(或C2H4O3)
B. 过氧乙酸是由碳、氢、氧三种元素构成的
C. 过氧乙酸中碳、氢、氧三种元素的质量比是12:1:16
D. 过氧乙酸中碳元素的质量分数是40%
【答案】A
【解析】
A、1个过氧乙酸分子是由2个碳原子、4个氢原子和3个氧原子构成的,则过氧乙酸的化学式是CH3COOOH(或C2H4O3),说法正确;故符合题意;
B、过氧乙酸是由碳、氢、氧三种元素组成的,说法错误;故不符合题意;
C、过氧乙酸中碳、氢、氧元素的质量比为(12×2):(1×4):(16×3)=6:1:12,说法错误;故不符合题意;
D、过氧乙酸中碳元素的质量分数是![]() ,说法错误;故不符合题意;
,说法错误;故不符合题意;
故选A

 同步轻松练习系列答案
同步轻松练习系列答案 课课通课程标准思维方法与能力训练系列答案
课课通课程标准思维方法与能力训练系列答案【题目】“双吸剂”是常用的袋装食品的保鲜剂,可用来吸收氧气、二氧化碳、水蒸气等气体。某化学小组的同学在袋装食品中发现一包名为“504双吸剂”的保鲜剂,其标签如图所示。同学们对这包久置的“504双吸剂”的固体样品很好奇,涉及实验进行探究。

(提出问题):久置固体的成分是什么?
(收集资料):
(1)查阅资料:铁与氯化铁溶液在常温下生成氯化亚铁:Fe+2FeCl3═3FeCl2
(2)打开固体包装观察:部分粉末呈黑色、部分粉末呈白色、另有少数红棕色的块状固体。
(作出猜想):久置固体中可能含有Fe、Fe2O3、CaO、Ca(OH)2、CaCO3.你猜想固体中可能含有Fe2O3的依据是_____。
(实验探究):如表是甲组同学涉及并记录的实验报告,请你补充完整。
实验操作 | 实验现象 | 实验结论 |
一、取少量固体加入足量蒸馏水,搅拌溶解 | 固体部分溶解,并放出大量热 | 固体中一定含有_____ |
二、过滤,取滤液滴加无色酚酞试液 | 溶液变红色 | 固体中一定含有氢氧化钙 |
三、取滤渣加入足量稀盐酸 | 固体逐渐消失,产生大量无色气体,得到浅绿色溶液 | 固体中一定含有_____,一定不含有Fe2O3 |
四、将操作三中产生的气体通入到澄清石灰水中 | 澄清石灰水变浑浊 | 固体中一定含有_____ |
(实验质疑):乙组同学认为甲组同学在实验中得出“一定不含有Fe2O3”的结论是错误的,理由是_____;你认为甲组同学哪一步操作得出的结论也不合理___,理由是(用化学方程式表示)_____。
(继续探究):为验证固体中是否含有Fe2O3,乙组同学用___先分离出铁粉,向残留固体中加入足量__,若溶液呈棕黄色,证明固体中含有Fe2O3.写出溶液呈棕黄色的化学反应方程式___。
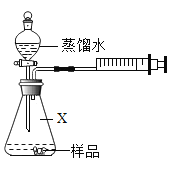
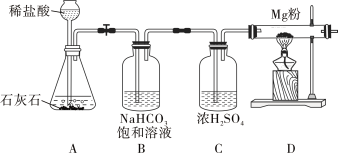
【题目】菱铁矿和赤铁矿一样,也是工业上冶炼铁的一种矿物。某种菱铁矿中铁元素的主要存在形式是碱式碳酸亚铁,为测定碱式碳酸亚铁[xFeCO3yFe(OH)2zH2O]的组成,华雪同在老师的指导下设计了如图实验装置:
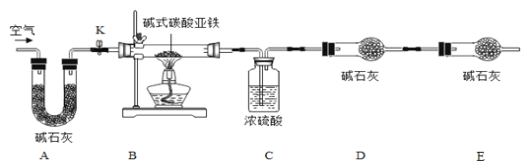
(查阅资料)
a.碱式碳酸亚铁受热会完全分解生成FeO、CO2以H2O。
b.FeO是一种黑色粉末,它不稳定,在空气中加热,可被氧化成四氧化三铁。
c.碱石灰是NaOH及CaO的混合物,可以吸收CO2和H2O
(实验步骤)
(1)检查装置的_____后,准备称取3.40g碱式碳酸亚铁粉末放在装置B中,连接仪器。
(2)_____,鼓入一段时间空气,准确称量装置C、D、E的质量。
(3)关闭弹簧夹K,加热装置B至装置C中导管末端无气泡冒出,再打开弹簧夹K,缓缓通空气一段时间,这样操作的目的是_____。
(4)再次准确称量装置C、D、E的质量,所得数据如下
装置C/g | 装置D/g | 装置E/g | |
加热前 | 200.00 | 180.00 | 180.00 |
加热后 | 200.36 | 180.88 | 180.00 |
(5)分析图、表中数据可知:3.40g碱式碳酸亚铁受热分解过程中生成H2O的质量为_____g,CO2的质量为_____g,装置E的作用是_____。
(实验结论)
在xFeCO3yFe(OH)2zH2O中,氢原子与氧原子的个数之比为_____。
(实验反思)
(1)装置A的作用是_____。
(2)实验结束后,装置B中的残留固体可能全部是FeO.也可能全部是Fe3O4.还可能是_____。
(3)为了得到装置B中残留固体的组成,华雪同学称得装置B中残留固体质量为2.24g后,通过计算可知:残留固体的组成及各成分的质量为_____。
【题目】某校兴趣小组在实验室中完成制取氧气的实验。它们取氯酸钾和二氧化锰的混合物共3.0克放入大试管中加热,并在不同时刻测定试管内剩余固体物质的质量(如下表):
反应时间/min | 1.0 | 1.5 | 2.0 | 2.5 | 3.0 |
剩余固体质量/g | 2.55 | 2.25 | 2.10 | 2.04 | 2.04 |
分析表中数据,完成下列问题:
(1)完全反应后,生成氧气多少克。
(2)原混合物中氯酸钾的质量分数是多少?