题目内容
葡萄糖(化学式为C6H12O6)是一种有甜味、易溶于水的白色粉末状固体.葡萄糖在人体内发生缓慢氧化转化为二氧化碳和水,并释放出热量.下面是有关葡萄糖的一些计算.(1)葡萄糖的相对分子质量是 ______;
(2)葡萄糖中各元素的最简质量比为C:H:O=______;
(3)葡萄糖中氢元素的质量分数为 ______(保留一位小数)
(4)一定量的葡萄糖溶解于水,得到的溶液中原子的个数比是H:O=______;
(5) 18g葡萄糖在人体完全氧化能产生多少克二氧化碳?(假如葡萄糖中的碳元素全部转化到二氧化碳中)
【答案】分析:(1)物质的相对分子质量为:该分子中的各元素的原子个数×相应的元素的相对原子质量;
(2)葡萄糖中各元素的最简质量比=(碳原子的个数×碳原子的相对原子质量):(氢原子的个数×氢原子的相对原子质量):(氧原子的个数×氧原子的相对原子质量);
(3)纯净物中某元素的质量分数= ×100%.
×100%.
(4)一定量的葡萄糖溶解于水,得到的溶液中:①水分子(H2O)中的氢、氧原子的个数比为2:1;②由葡萄糖(化学式为C6H12O6)可知:物质C6H12O6中的氢、氧原子的个数比为2:1;故可知一定量的葡萄糖溶解于水,得到的溶液中氢、氧原子的个数比;
(5)①方法1:书写化学方程式C6H12O6+6O2=6CO2+6H2O,可利用化学方程式计算,求解,得出二氧化碳的质量;
②方法2:可求出18g葡萄糖中的碳元素的质量,已知葡萄糖中的碳元素全部转化到二氧化碳中,再利用二氧化碳中的碳元素的质量分数可求出产生的二氧化碳的质量.
解答:解:(1)葡萄糖的相对分子质量为12×6+1×12+16×6=180;
(2)葡萄糖中各元素的最简质量比为:C:H:O=(12×6):(1×12):(16×6)=6:1:8
(3)葡萄糖中氢元素的质量分数为;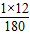 ≈6.7%
≈6.7%
(4)一定量的葡萄糖溶解于水,得到的溶液中原子的个数比是H:O=12:6=2:1
(5)设18g葡萄糖在人体完全氧化能产生x克二氧化碳,
故可列式为:18× ×100%=
×100%= ×100%x,解得x=26.4g
×100%x,解得x=26.4g
故答为:(1)180,(2)6:1:8,(3)6.7%,(4)2:1,(5)26.4g
点评:要求掌握并理解各元素的相对原子质量的作用;求物质中各元素的比值,计算某分子的相对分子质量,求某物质中某元素的质量分数都是基本的计算.
(2)葡萄糖中各元素的最简质量比=(碳原子的个数×碳原子的相对原子质量):(氢原子的个数×氢原子的相对原子质量):(氧原子的个数×氧原子的相对原子质量);
(3)纯净物中某元素的质量分数=
 ×100%.
×100%.(4)一定量的葡萄糖溶解于水,得到的溶液中:①水分子(H2O)中的氢、氧原子的个数比为2:1;②由葡萄糖(化学式为C6H12O6)可知:物质C6H12O6中的氢、氧原子的个数比为2:1;故可知一定量的葡萄糖溶解于水,得到的溶液中氢、氧原子的个数比;
(5)①方法1:书写化学方程式C6H12O6+6O2=6CO2+6H2O,可利用化学方程式计算,求解,得出二氧化碳的质量;
②方法2:可求出18g葡萄糖中的碳元素的质量,已知葡萄糖中的碳元素全部转化到二氧化碳中,再利用二氧化碳中的碳元素的质量分数可求出产生的二氧化碳的质量.
解答:解:(1)葡萄糖的相对分子质量为12×6+1×12+16×6=180;
(2)葡萄糖中各元素的最简质量比为:C:H:O=(12×6):(1×12):(16×6)=6:1:8
(3)葡萄糖中氢元素的质量分数为;
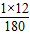 ≈6.7%
≈6.7%(4)一定量的葡萄糖溶解于水,得到的溶液中原子的个数比是H:O=12:6=2:1
(5)设18g葡萄糖在人体完全氧化能产生x克二氧化碳,
故可列式为:18×
 ×100%=
×100%= ×100%x,解得x=26.4g
×100%x,解得x=26.4g故答为:(1)180,(2)6:1:8,(3)6.7%,(4)2:1,(5)26.4g
点评:要求掌握并理解各元素的相对原子质量的作用;求物质中各元素的比值,计算某分子的相对分子质量,求某物质中某元素的质量分数都是基本的计算.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
 6CO2+6H2O(反应中每克葡萄糖放出热量15.6kJ)
6CO2+6H2O(反应中每克葡萄糖放出热量15.6kJ) 6CO2+6H2O(反应中每克葡萄糖放出热量15.6kJ)
6CO2+6H2O(反应中每克葡萄糖放出热量15.6kJ)