题目内容
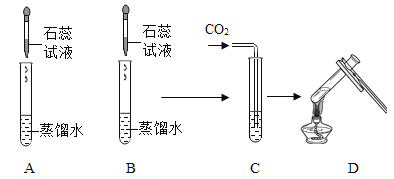
【题目】结合下列验证氢氧化钙化学性质的实验图示,回答有关问题:
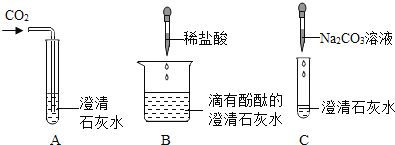
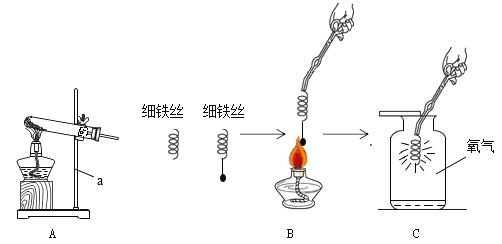
(1)实验A中一定能够观察到的明显现象是_________。
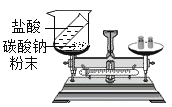
(2)实验B验证了氢氧化钙能与____________、_________(填物质的类别)作用。
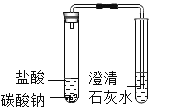
(3)实验C中发生的反应可用化学方程式表示为__________。
(4)将A、B、C三个实验后的所有物质倒入同一个烧杯中,发现有气泡产生,最后只得到了无色溶液,则最后得到的无色溶液中一定含有的溶质是__________(指示剂除外)。
【答案】澄清石灰水变浑浊 酸碱指示剂 酸 Na2CO3+Ca(OH)2=CaCO3↓+2NaOH CaCl2、NaCl
【解析】
(1)因为二氧化碳能和氢氧化钙反应生成难溶于水的碳酸钙,所以实验A中一定能够观察到的明显现象是:澄清石灰水变浑浊。
(2)实验B操作过程中,首先向澄清石灰水中滴加几滴无色酚酞溶液,氢氧化钙溶液具有碱性,能与酚酞作用使酚酞变红,溶液呈红色;滴入稀盐酸后,溶液由红色变为无色,说明氢氧化钙能与盐酸发生中和反应。因此实验B验证了氢氧化钙能与酸碱指示剂、酸作用。
(3)碳酸钠溶液和澄清石灰水反应生成碳酸钙和氢氧化钠,因此实验C中发生的反应可用化学方程式表示为:Na2CO3+Ca(OH)2=CaCO3↓+2NaOH。
(4)将A、B、C三个实验后的所有物质倒入同一个烧杯中,发现有气泡产生,最后只得到了无色溶液。因为最后只得到溶液,所以烧杯中没有碳酸钙,碳酸钙和稀盐酸反应生成氯化钙;因为溶液中存在酚酞,最后得到的是无色溶液,可见溶液不呈碱性,所以溶液中不含碳酸钠、氢氧化钙、氢氧化钠等物质(即使在A、C实验中有剩余,混合后B实验中过量的稀盐酸也将它们反应完,实验B中盐酸一定过量,如果盐酸不过量,A、B、C三个实验后的所有物质倒入同一个烧杯中,就不会有气泡产生,当然混合后盐酸是否过量无法确定),碳酸钠、氢氧化钠和稀盐酸反应生成氯化钠,氢氧化钙和稀盐酸反应生成氯化钙。因此最后得到的无色溶液中一定含有的溶质是:CaCl2、NaCl(指示剂除外)。