题目内容
尿素[CO(NH2)2]是农业上重要的高效氮肥,计算:
①尿素的相对分子质量.
②尿素中各元素的质量比(按C、O、N、H的顺序).
③尿素中氮元素的质量分数.
①尿素的相对分子质量.
②尿素中各元素的质量比(按C、O、N、H的顺序).
③尿素中氮元素的质量分数.
考点:相对分子质量的概念及其计算,元素质量比的计算,元素的质量分数计算
专题:化学式的计算
分析:①根据相对分子质量为构成分子的各原子的相对原子质量之和,进行分析解答.
②根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
③根据化合物中元素的质量分数=
×100%,进行分析解答.
②根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
③根据化合物中元素的质量分数=
| 相对原子质量×原子个数 |
| 相对分子质量 |
解答:解:①尿素的相对分子质量=12+16+(14+1×2)×2=60.
②尿素中C、O、N、H元素的质量比为12:16:(14×2):(1×2×2)=3:4:7:1.
③尿素中氮元素的质量分数为
×100%≈46.7%.
答:①尿素的相对分子质量为60;②尿素中C、O、N、H元素的质量比等于3:4:7:1;③尿素中氮元素的质量分数为46.7%.
②尿素中C、O、N、H元素的质量比为12:16:(14×2):(1×2×2)=3:4:7:1.
③尿素中氮元素的质量分数为
| 14×2 |
| 60 |
答:①尿素的相对分子质量为60;②尿素中C、O、N、H元素的质量比等于3:4:7:1;③尿素中氮元素的质量分数为46.7%.
点评:本题难度不大,考查同学们灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
相关题目
下列各组物质,前者属于纯净物,后者属于混合物的是( )
| A、氧气、二氧化碳 |
| B、澄清石灰水、冰水混合物 |
| C、红磷、五氧化二磷 |
| D、蒸馏水、空气 |
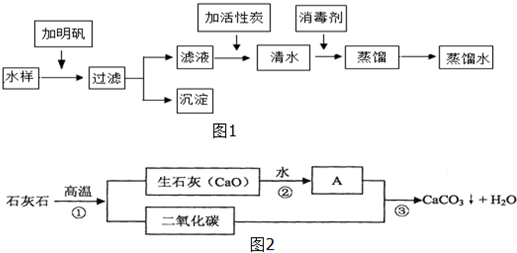
 根据图中信息回答下列问题:
根据图中信息回答下列问题: