题目内容
【题目】某化学兴趣小组欲测定碳酸钙样品的纯度(杂质不与盐酸反应)取 12.5g 样品加入到稀 盐酸中,产生 CO2 的质量与稀盐酸的质量关系如图所示,
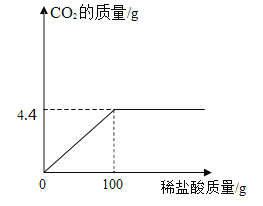
请回答:
(1)该实验最多制得 CO2 的质量为 g
(2)该碳酸钙样品的纯度为
(3)计算所加稀盐酸的溶质质量分数。(要求有计算过程)
【答案】(1) 4.4 g (2) 80%
(3)CaCO3 + 2HCl= CaCl2 + H2O + CO2↑
100 7 3 44
x y 4.4g
100/x=73/y=44/4.4g
x=10g ,y=7.3g
CaCO3%=10/12.5×100%=80%
HCl%=7.3/100×100%=7.3%
【解析】碳酸钙与稀盐酸反应生成氯化钙、水和二氧化碳。利用化学方程式,根据二氧化碳与碳酸钙反应的质量比即可计算出碳酸钙的质量和稀盐酸中溶质的质量。
由图可知,生成的二氧化碳的质量为4.4g;
设样品中碳酸钙的质量为x,稀盐酸中溶质的质量为y;
CaCO3 + 2HCl= CaCl2 + H2O + CO2↑
100 73 44
X y 4.4g
![]() x=10g
x=10g
![]()
![]() y=7.3g
y=7.3g
该碳酸钙样品的纯度=![]() 80%
80%
所加稀盐酸的溶质质量分数=![]() 7.3%
7.3%
答:略

练习册系列答案
相关题目
【题目】在一密闭容器中加入甲、乙、丙、丁四种物质,一定条件下充分反应,反应前后的数据如下表。下列说法正确的是
物质的质量 | 甲 | 乙 | 丙 | 丁 |
反应前 | 25g | 8 g | X | 5g |
反应后 | 8g | 8g | 20g | 9g |
A. x=6g B. 甲的化学计量数等于丙和丁的化学计量数之和
C. 乙物质一定是催化剂 D. 该反应是分解反应