题目内容
29、化学兴趣小组的同学为探究铁、铜、锌、银的金属活动性顺序,设计了如图1三个实验(其中金属均已打磨、其形状、大小及同种稀盐酸的用量均相同).

(1)小明同学认为通过①和③可以比较铁和锌的金属活动性,他依据的实验现象是
(2)一段时间后,观察到②中的铜片表面有银白色固体附着,这说明铜比银的活泼性
(3)小红认为上述实验方案不足以得出四种金属的活动性顺序,并在上述实验的基础上,利用金属不同的化学性质补充了一个实
验(图2所示),从而达到了实验探究目的.则小红同学的实验中:x是金属

(1)小明同学认为通过①和③可以比较铁和锌的金属活动性,他依据的实验现象是
锌与稀盐酸反应产生气泡的速率比铁快
;(2)一段时间后,观察到②中的铜片表面有银白色固体附着,这说明铜比银的活泼性
强
(填“强”或“弱”).该反应的化学方程式为Cu+2AgNO3═Cu(NO3)2+2Ag
.(3)小红认为上述实验方案不足以得出四种金属的活动性顺序,并在上述实验的基础上,利用金属不同的化学性质补充了一个实
验(图2所示),从而达到了实验探究目的.则小红同学的实验中:x是金属
Fe(铁)或Cu(铜),
;y是CuSO4(硫酸铜)或HCl(稀盐酸)
溶液.分析:根据题意可知本题比较金属的活泼性,主要是利用了金属与酸、与盐溶液的反应来得出结论的.Zn、Fe都与盐酸反应但快慢不同,Cu能与硝酸银溶液反应置换出Ag,难点是怎么比较Fe和Cu,需另设计实验,但出发点仍是利用金属与酸、与盐溶液的反应.
解答:解:
(1)通过实验①和③的现象可知,锌与稀盐酸反应产生气泡的速度比铁的快,Zn与盐酸反应剧烈,
锌的金属活动性比铁强;
(2)通过观察到实验②的铜片表面有银白色固体附着,可知银白色固体为银,铜与与硝酸银溶液反应生成了银,所以铜比银活泼,化学方程式为,Cu+2AgNO3=Cu(NO3)2+2Ag;
(3)根据以上实验只能得出金属的活泼性Zn>Fe,Cu>Ag,关键是比较Fe>Cu,若是利用金属与盐溶液反应,可设计让铁与含Cu2+的溶液反应,X是Fe(或铁),Y是CuSO4(硫酸铜);若是利用金属与酸反应,可设计铜与稀酸反应,因为铁能与酸反应,当看到铜不与稀酸反应,就可得出活泼性Fe>Cu,X是Cu(或铜),Y是HCI(或稀盐酸).
故答案为:
(1)锌与稀盐酸反应产生气泡的速率比铁快;
(2)强,Cu+2AgNO3═Cu(NO3)2+2Ag;
(3)Fe(铁)或Cu(铜),CuSO4(硫酸铜)或HCl(稀盐酸).
(1)通过实验①和③的现象可知,锌与稀盐酸反应产生气泡的速度比铁的快,Zn与盐酸反应剧烈,
锌的金属活动性比铁强;
(2)通过观察到实验②的铜片表面有银白色固体附着,可知银白色固体为银,铜与与硝酸银溶液反应生成了银,所以铜比银活泼,化学方程式为,Cu+2AgNO3=Cu(NO3)2+2Ag;
(3)根据以上实验只能得出金属的活泼性Zn>Fe,Cu>Ag,关键是比较Fe>Cu,若是利用金属与盐溶液反应,可设计让铁与含Cu2+的溶液反应,X是Fe(或铁),Y是CuSO4(硫酸铜);若是利用金属与酸反应,可设计铜与稀酸反应,因为铁能与酸反应,当看到铜不与稀酸反应,就可得出活泼性Fe>Cu,X是Cu(或铜),Y是HCI(或稀盐酸).
故答案为:
(1)锌与稀盐酸反应产生气泡的速率比铁快;
(2)强,Cu+2AgNO3═Cu(NO3)2+2Ag;
(3)Fe(铁)或Cu(铜),CuSO4(硫酸铜)或HCl(稀盐酸).
点评:本题考查了学生的实验设计能力,属于能力提高型习题,且本题具有开放性,学生的思维空间较大,如(3)中Y的选择,能培养学生创新设计的能力.开放型习题有助于学生对知识的综合应用.

练习册系列答案
相关题目
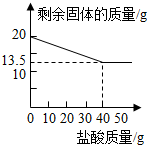 某化学兴趣小组的同学为测定假黄金(铜锌合金)组成元素的质量分数,称取20克假黄金置于烧杯中,用某浓度的稀盐酸50克,分5次加入,每次充分反应后,取出固体,经过滤、干燥等操作后称量,5次稀盐酸用量和剩余固体质量记录如下:
某化学兴趣小组的同学为测定假黄金(铜锌合金)组成元素的质量分数,称取20克假黄金置于烧杯中,用某浓度的稀盐酸50克,分5次加入,每次充分反应后,取出固体,经过滤、干燥等操作后称量,5次稀盐酸用量和剩余固体质量记录如下:| 实验次数 | 稀盐酸的用量(g) | 剩余固体的质量(g) |
| 1 | 10 | 18.375 |
| 2 | 10 | 16.750 |
| 3 | 10 | 15.125 |
| 4 | 10 | 13.500 |
| 5 | 10 | 13.500 |
(2)计算稀盐酸中溶质的质量分数;
(3)当合金中的锌与稀盐酸恰好完全反应时,所得溶液中溶质的质量分数为多少?
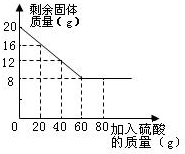 某化学兴趣小组的同学为测定Cu和CuO混合样品中CuO的含量,甲、乙、丙、丁四位同学均先称取20g样品于烧杯中,在分别加入20g、40g、60g、80g溶质质量分数相同的稀硫酸.充分反应后,均有固体剩余.经过滤、干燥后称量,剩余固体质量如下图所示.回答下列问题:
某化学兴趣小组的同学为测定Cu和CuO混合样品中CuO的含量,甲、乙、丙、丁四位同学均先称取20g样品于烧杯中,在分别加入20g、40g、60g、80g溶质质量分数相同的稀硫酸.充分反应后,均有固体剩余.经过滤、干燥后称量,剩余固体质量如下图所示.回答下列问题: