题目内容
【题目】如图是按顺序分别是锂、钠、氮、磷、和氧的一种微粒的结构示意图,回答下列问题:
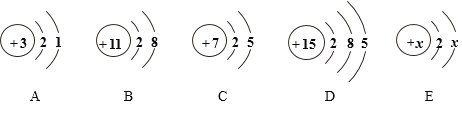
(1)B粒子属于________(填“原子”“阴离子”或“阳离子”)。
(2)与C粒子化学性质相似的是__________(填字母序号)。
(3)写出含有D的氧化物是__________。
(4)在E的粒子中,x=_________,其符号是_________。
(5)锂广泛应用于电池、贮氢等领域,锂元素在化合物中显+1价。锂元素在元素周期表中的信息如图所示。

①从图中的数值获得的一条信息是________。
②LiMnO4是一种电极材料,其中Mn元素的化合价为_________。
③氢氧化锂的化学式为_________。
【答案】阳离子 D P2O5 8 O2- 锂元素的相对原子质量为6.941 +7 LiOH
【解析】
(1)B粒子表示一个钠原子失去一个电子,形成带一个单位正电荷的钠离子,属于阳离子。
(2)原子最外层电子数相等,化性质相似;C粒子最外层有5个电子,与其化学性质相似的是D,最外层同样有5个电子。
(3)D中含有15个质子,表示磷元素,其氧化物是:P2O5;
(4)在E的粒子中,核内有x个质子,且最外层电子数为x,则表示该粒子得到两个电子,x=8,其符号是:O2-;
(5)①从图中的数值获得的一条信息是:锂元素的相对原子质量为6.941;锂元素是金属元素;锂的元素符号为:Li ;
②LiMnO4是一种电极材料,其中锂元素为+1价,氧元素为-2价,设:Mn元素的化合价为x,则(+1)+x+(-2)×4=0,x=+7;
③氢氧化锂中锂元素为+1价,氢氧根为-1价,则化学式为:LiOH。

 名校作业本系列答案
名校作业本系列答案 轻巧夺冠周测月考直通名校系列答案
轻巧夺冠周测月考直通名校系列答案【题目】中医药是中华文明的重要组成部分。中医药在2020抗击新冠肺炎“战疫”中起重要的作用。初中常见的很多化学物质都是中医常用的药物。芒硝的主要成分是硫酸钠,在中医药中常用于湿热积滞、腹满胀痛、大便燥结等病症治疗。芒硝广泛分布于我国各地,尤其以盐碱地分布较多。
小青和小竹在了解芒硝的基本信息后,准备用盐湖水制备少量的Na2SO4晶体。
[查阅资料]
I.盐湖水中的溶质是NaCl、Na2CO3和Na2SO4.
II. NaCl、Na2CO3和Na2SO4在水中不同温度下的溶解度如下表所示:
0°C | 10°C | 20°C | 30°C | 40°C | |
NaCl | 35.7g | 35.8g | 36.0g | 36.3g | 36.6g |
Na2CO3 | 7g | 12.2g | 21.8g | 39.7g | 48.8g |
Na2SO4 | 4.9g | 9.1g | 19.5g | 40.8g | 48.8g |
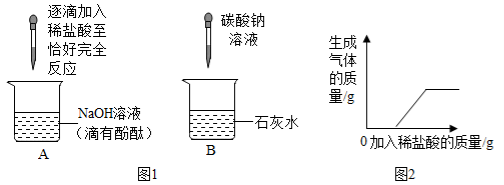
(1)若要证明盐湖水中含有NaCl、Na2CO3 和Na2SO4,可依次加入适量的__________(选填字母),看到相应现象即可证明.
A AgNO3、H2SO4、BaCl2
B HCl、Ba(NO3)2、AgNO3
C HNO3、Ba(NO3)2、AgNO3
[进行实验]用盐湖水制取少量Na2SO4晶体
小青方案 | 取少盐湖水,蒸发浓缩,降温结晶,过滤,洗涤,干燥 |
[实验讨论]
(2)同学们讨论后认为小青的方案存在问题,因为用小青的方案得到的晶体除了含有硫酸钠外,还含有____晶体杂质。小竹在小青方案的基础上进行了改进,从而达到实验目的,
(3)小青的实验方案中“洗涤晶体”这一操作最好使用饱和_____________溶液洗而不用水洗,以防止硫酸钠固体溶于水造成晶体的损失。
[实验拓展]小湖同学想通过实验测得一定质盐湖水中Na2CO3的溶质质量分数,设计了下图所示装置进行实验,通过测定装D中氢氧化钠溶液的质量变化。然后计算,从而达到实验目的。
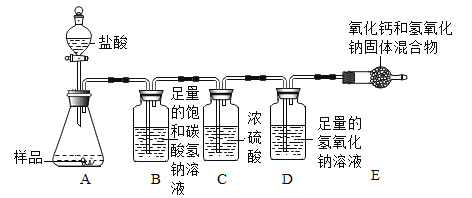
(4)装置B的作用是:_______________________。
(5)若将装置C和D颠倒位置,则通过计算得出Na2CO3的溶质质量分数__________ (填“偏大”、 “偏小”或“无影响”) .
【题目】小敏同学发现:向鱼池中撒入名为过氧化钙(化学式为CaO2)的固体物质时水面会出现一些气泡,为此他进行了如下探究:
(提出问题)当把过氧化钙投入足量水中时,生成的气体是什么?
(进行猜想)①是氢气;②是________。
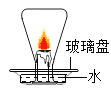
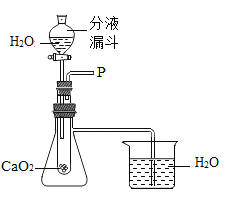
(实验探究)小敏设计如图所示的装置进行探究。他打开装置中分液漏斗的活塞,观察到试管内有气泡产生,反应一段时间后,做了以下两步操作:
步骤 | 实验操作 | 实验现象 | 实验结论 |
一 | 将燃着的木条放在导管口P处 | 没有看到气体燃烧,但木条燃烧更旺盛。 | 猜想①错误 |
二 | 将带火星的木条放在导管口P处 | ____________________。 | 猜想②正确 |
(问题讨论)
(1)实验时烧杯中也有气泡出现,说明该反应发生时会________(填“放热”或“吸热”);
(2)通过探究实验可以得知过氧化钙的正确保存方法是______________;
(3)人们在运输鱼苗时,常会在水中加入少量过氧化钙,其主要目的是___________。
【题目】2020年1月25日总建筑面积为3.39万平方米的火神山医院正式开工,火神山医院在建造过程中用到/HDPE膜。HDPE膜具有极好的抗冲击性和防潮性,听完老师的描述后,同学们对HDPE膜的组成元素产生了浓厚的兴趣,进行了如下探究。
(提出问题)HDPE膜由什么元素组成?
(查阅资料)
①HDPE膜能够燃烧,燃烧可能生成一氧化碳。
②碱石灰主要成分是氢氧化钠固体和氧化钙固体。
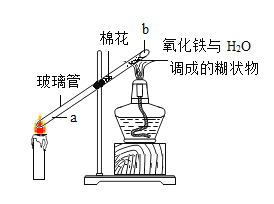
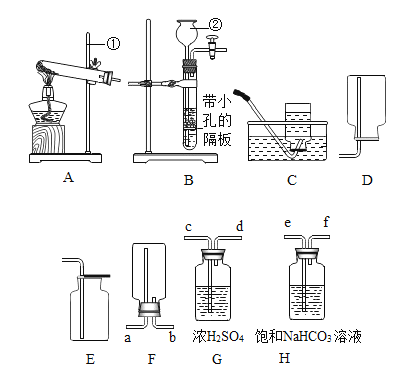
(实验探究)如图所示,先通入干燥氮气,再将4.2g的HDPE膜样品在一定质量的氧气中点燃,并将燃烧产物依次通过装置A、B、C、D (装置中每步反应均进行完全)。
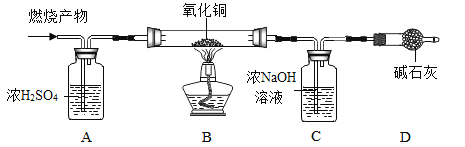
(实验记录)
装置质量 | A装置总质量 | C装置总质量 |
实验前 | 100.0g | 100.0g |
实验后 | 105.4g | 113.2g |
(实验分析)
(1)装置.A中浓硫酸的作用是___________。
(2)当观察到装置B中黑色粉末变成___色,可证明HDPE膜的燃烧产物中有_______。
(3)装置C中发生的化学反应方程式为________________。
(4)装置D的作用是________________。
(实验结论)
HDPE膜由元素_________(填元素符号)组成,它们的原子个数比为______。
(装置优化)
有同学认为,如若操作不当,C中溶液有可能会倒吸回B装置中,使得硬质玻璃管因骤冷而破裂为了降低实验风险,需要进行装置优化,请在方框中画出图像_________。