题目内容
【题目】20℃时,将等质量不含结晶水的甲、乙固体分别加入到盛有100g水的烧杯中,充分搅拌后现象如图1,加热到50℃时现象如图2(不考虑水分蒸发),甲、乙固体的溶解度曲线如图3. 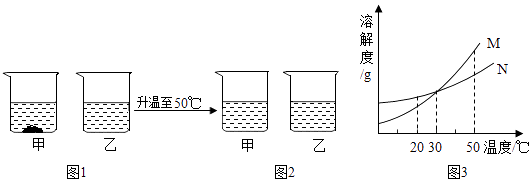
(1)图1中,一定是饱和溶液是 .
(2)图2中,两溶液中溶质的质量分数甲乙(填“>”、“<”、“=”).
(3)图3中,表示甲的溶解度曲线的是(填字母编号)
(4)若使图2中乙溶液析出较多晶体应采取的结晶方法是 .
【答案】
(1)甲
(2)=
(3)M
(4)蒸发结晶
【解析】解:(1)图1中甲有溶质剩余,甲一定是饱和溶液;故填:甲;(2)图2中均无固体剩余,说明全部溶解,相同质量的溶剂溶解了相同质量的溶质,所以图2中,两溶液中溶质的质量分数相等;故填:=;(3)根据图1中信息可以知道20℃时甲的溶解度小于乙的溶解度,而图3中在20℃时,N曲线的溶解度大于M曲线的溶解度,故表M示的是甲物质的溶解度曲线;故填:M.(4)图3可知乙物质的溶解度受温度的影响变化不大,所以若使图2中乙溶液析出较多晶体应采取的结晶方法是蒸发结晶.故填:蒸发结晶.
【考点精析】本题主要考查了结晶的原理、方法及其应用和饱和溶液和不饱和溶液的相关知识点,需要掌握结晶的两种方法:蒸发溶剂,如NaCl(海水晒盐)和降低温度(冷却热的饱和溶液,如KNO3);饱和与不饱和的判断方法:看有无不溶物或继续加入该溶质,看能否溶解才能正确解答此题.

练习册系列答案
相关题目