题目内容
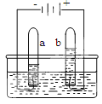
【题目】(5分,第4小题2分)如图中A、B分别是某微粒的结构示意图,回答下列问题:
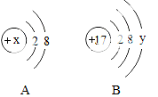
(1)若A是某阴离子的结构示意图,则x可能是下列中的 _________ (填字母序号)
a.8 b.10 c.11 d.12
(2)若B表示某原子的结构示意图,则y= _________ 。
(3)若A中x=12,则A、B所表示的元素形成化合物的名称为 _________ 。
(4)稀土元素是一类有重要用途的资源。铈(Ce)是一种常见的稀土元素,下列有关说法正确的是
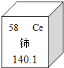
A.铈的原子序数是58 B.铈属于非金属元素
C.铈原子中的质子数是58 D.铈的相对原子质量是140.1
【答案】(1)a (2)7 (3)氯化镁 (4)ACD
【解析】
试题分析:(1)当质子数<电子数,为阴离子,若A是某阴离子的结构示意图,则x可能是下列中的a
(2)当质子数=电子数,为原子,故若B表示某原子的结构示意图,则y=17-2-8=7
(3)若A中x=12,为镁元素,B为氯元素,故A、B所表示的元素形成化合物的名称为氯化镁
(4)根据元素周期表中的信息可知:铈的原子序数是58,铈原子中的质子数是58,铈的相对原子质量是140.1;铈带“金字旁”,属于金属元素,错误,故选ACD

练习册系列答案
相关题目