��Ŀ����
�������������������Ź㷺��Ӧ�ã�
��1�����йر�����ÿ������ʴ�����ϵ�����ƷԼռ�������20%��40%������Ʒ������������� ����
��2��д����ϡ���������Ļ�ѧ����ʽ�� ����
��3��ͬѧ��ͨ��ʵ������֤Cu��Fe��Ag���ֽ����Ļ��˳��ʵ�����ṩ��ҩƷ�У�
Cu��NO3��2��Һ��AgNO3��Һ��Fe��NO3��2��Һ��ϡ���ᡢͭ˿����˿����˿��
��С��ͬѧ��Ʋ����������ʵ�飺
�ٰ���˿����װ��ϡ������Թ��У� �ڰ�ͭ˿����װ��ϡ������Թ��У�
�۰���˿����װ��ϡ������Թ��У� �ܰ�ͭ˿����װ��AgNO3��Һ���Թ��У�
�۲쵽���е�ʵ���������� �������еĻ�ѧ����ʽ���� ��������ΪС��������ʵ������������ţ��Ƕ���ģ�
������С��ֻѡ��������ҩƷ�е����֣�ͨ������ʵ�飬Ҳ�ﵽ��ʵ��Ŀ�ģ���ѡ�õ�����ҩƷ���� ����д��һ��ҩƷ��ϼ��ɣ���
��1�����йر�����ÿ������ʴ�����ϵ�����ƷԼռ�������20%��40%������Ʒ������������� ����
��2��д����ϡ���������Ļ�ѧ����ʽ�� ����
��3��ͬѧ��ͨ��ʵ������֤Cu��Fe��Ag���ֽ����Ļ��˳��ʵ�����ṩ��ҩƷ�У�
Cu��NO3��2��Һ��AgNO3��Һ��Fe��NO3��2��Һ��ϡ���ᡢͭ˿����˿����˿��
��С��ͬѧ��Ʋ����������ʵ�飺
�ٰ���˿����װ��ϡ������Թ��У� �ڰ�ͭ˿����װ��ϡ������Թ��У�
�۰���˿����װ��ϡ������Թ��У� �ܰ�ͭ˿����װ��AgNO3��Һ���Թ��У�
�۲쵽���е�ʵ���������� �������еĻ�ѧ����ʽ���� ��������ΪС��������ʵ������������ţ��Ƕ���ģ�
������С��ֻѡ��������ҩƷ�е����֣�ͨ������ʵ�飬Ҳ�ﵽ��ʵ��Ŀ�ģ���ѡ�õ�����ҩƷ���� ����д��һ��ҩƷ��ϼ��ɣ���
��1����������ˮͬʱ�Ӵ� ��2��6HCl+Fe2O3�T2FeCl3+3H2O
��3������˿���������ݲ�������Һ����ɫ��Ϊdz��ɫ Cu+2AgNO3�T2Ag+Cu��NO3��2 ��
��ͭ˿��Ag NO3��Һ��Fe��NO3��2��Һ
��3������˿���������ݲ�������Һ����ɫ��Ϊdz��ɫ Cu+2AgNO3�T2Ag+Cu��NO3��2 ��
��ͭ˿��Ag NO3��Һ��Fe��NO3��2��Һ
�����������1������Ʒ�������������������ˮͬʱ�Ӵ���
�����������ˮͬʱ�Ӵ���
��2����ϡ���������Ļ�ѧ����ʽΪ��6HCl+Fe2O3�T2FeCl3+3H2O��
���6HCl+Fe2O3�T2FeCl3+3H2O��
��3�������ܺ�ϡ���ᷴӦ�����Ȼ��������������Ȼ�������Һ��dz��ɫ�ģ��۲쵽���е�ʵ����������˿���������ݲ�������Һ����ɫ��Ϊdz��ɫ��
�����˿���������ݲ�������Һ����ɫ��Ϊdz��ɫ��
ͭ��������ǰ�棬�ܺ���������Һ��Ӧ������������ͭ����Ӧ�Ļ�ѧ����ʽΪ��Cu+2AgNO3�T2Ag+Cu��NO3��2��
���Cu+2AgNO3�T2Ag+Cu��NO3��2��
�ɢ٢ڿ�֪������ͭ���ã��ɢܿ�֪��ͭ�������ã����Ԣ��Ƕ���ģ�
����ۣ�
����ͭ˿��Ag NO3��Һ��Fe��NO3��2��Һ���Լ�������ͭ�����Ļ�����˳��ͭ˿������������Һ��ʱ��ͭ˿���渽����һ������ɫ���ʣ�˵��ͭ�������ã���ͭ˿��������������Һ��ʱ������������˵������ͭ���ã��ɷ�����֪�����ֽ����Ļ������ǣ�����ͭ���ã�ͭ�������ã�
���ͭ˿��Ag NO3��Һ��Fe��NO3��2��Һ��
������������Ҫ�������������������ѧ����ʽ����д���������˳����жϵȷ����֪ʶ����д��ѧ����ʽʱҪע���IJ���һ�Ƿ�Ӧ���������Ļ�ѧʽҪ��ȷ��������ѭ�����غ㶨�ɣ�����д�ϱ�Ҫ�����������ǿ��Ƿ��С�����������

��ϰ��ϵ�д�
 �·Ƿ��̸����100��ϵ�д�
�·Ƿ��̸����100��ϵ�д�
�����Ŀ

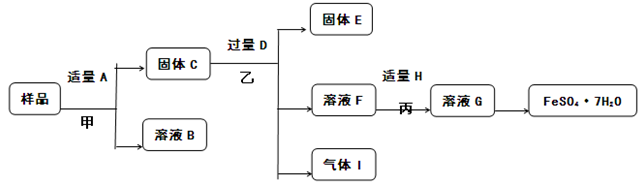
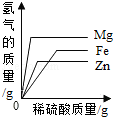
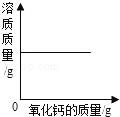


 ���ˣ����õ�����ϴ�ӡ�����������Ƶ�����Ϊa�ˣ�
���ˣ����õ�����ϴ�ӡ�����������Ƶ�����Ϊa�ˣ� ���ˣ����õ��Ĺ���ϴ�ӡ�����������Ƶ�����Ϊb�ˣ�
���ˣ����õ��Ĺ���ϴ�ӡ�����������Ƶ�����Ϊb�ˣ�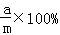 ��
�� ��
��



