题目内容
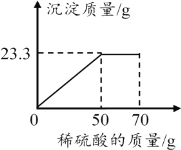
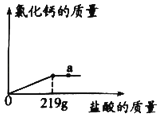
【题目】实验室模拟高温煅烧石灰石的方法制取二氧化碳,取35g石灰石样品(假设杂质受热不分解且不与酸反应),煅烧一段时间恢复到室温,测得生成1lg二氧化碳。向剩余固体中逐滴加入某盐酸至不再反应为止,又生成2.2g二氧化碳,加入盐酸的质量与生成的氯化钙质量关系如图:
. 
(1)石灰石样品的质量分数是_____(结果保留一位小数,下同);
(2)a点溶液的pH_____7(填“<”“>”或“=”);
(3)求所加盐酸的溶质质量分数_____(写出计算过程)。
【答案】85.7% < 10.0%
【解析】
根据生成的二氧化碳的质量和对应的化学方程式求算样品中碳酸钙的质量,以及根据钙元素和氯元素守恒求算消耗的所加盐酸的溶质质量分数。
(1)设样品中碳酸钙的质量为x,根据碳酸钙中的碳元素最终转化为二氧化碳中的碳元素可得关系式为:
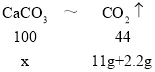
![]()
x=30g
石灰石样品的质量分数为:![]() ;故填:85.7%
;故填:85.7%
(2)a点时氯化钙质量已经不增加,说明盐酸过量,此时溶液显酸性,pH<7。故填:<
(3)设所加盐酸的溶质质量分数为y
根据钙元素和氯元素守恒可得关系式为
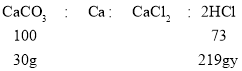
![]()
y=10.0%
故填:10.0%

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目