��Ŀ����
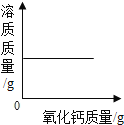
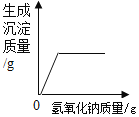
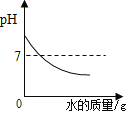
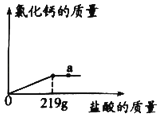
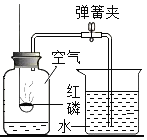
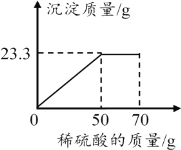
����Ŀ��ij���������п��ܺ���NaCl��BaCl2��NaOH�е�һ�ֻ��֡�ijУ����С��ͬѧΪ��̽����ɷ֣�ȡ�ù�������30g��ȫ����ˮ�У������Һ��pHΪ7��Ȼ��70gijϡ����������Һ�У���ַ�Ӧ�����������������������Ĺ�ϵ��ͼ��ʾ�������ͼʾ�����֪ʶ�ش����⡣
��1���ù���������һ�������е�������________����ѧʽ����
��2��ͨ������ȷ���������ʵ���ɳɷּ�����Ϊ_____��
��3������ϡ���������ʵ�����������_____��
���𰸡�NaOH BaCl2 20.8g��NaCl 9.2g 19.6%
��������
��1����Һ��pHΪ7��˵����Һ�����ԣ����в�����NaOH��
��2����70gijϡ����������Һ�У����ɲ�������ij�������˵����Һ�к���BaCl2�������ɳ���BaSO423.3g�����躬��BaCl2x����������y
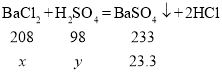
![]()
x=20.8g��y=9.8g
�ҹ�������������Ϊ30g��
����BaCl220.8g������NaCl 9.2g
��3������Ӧͼ���֪����Ӧ��ȫ��������50g
��ϡ���������ʵ�����������![]() ��
��

��ϰ��ϵ�д�
 ѧ���쳵�����ּ��������ҵ�½����������ϵ�д�
ѧ���쳵�����ּ��������ҵ�½����������ϵ�д� �����ѧСѧ�꼶�νӵ������㽭��ѧ������ϵ�д�
�����ѧСѧ�꼶�νӵ������㽭��ѧ������ϵ�д� Сѧ�����ҵ���ϴ�ѧ������ϵ�д�
Сѧ�����ҵ���ϴ�ѧ������ϵ�д� ���Ž�����ٰθ��νӹ㶫���������ϵ�д�
���Ž�����ٰθ��νӹ㶫���������ϵ�д�
�����Ŀ