题目内容
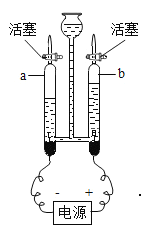
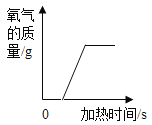
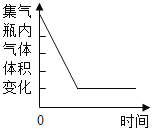
【题目】甲、乙、丙三种物质均含地壳中含量最多的元素。甲、乙是组成元素完全相同的化合物,且常温下都是液体;丙是单质;它们之间有如右图所示的转化关系(部分物质和反应条件已经略去)。
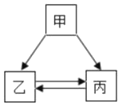
(1)甲分解成生成乙和丙的化学方程式为____________________。
(2)从微观角度解释甲、乙性质有些差异的原因是____________________。
【答案】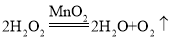 构成分子不同
构成分子不同
【解析】
甲、乙、丙三种物质均含地壳中含量最多的元素,则均含有氧元素。甲、乙是组成元素完全相同的化合物,且常温下都是液体,则是水和过氧化氢中的一种;甲能够转化为乙,则甲是过氧化氢,丙是单质,甲生成乙和丙,丙是氧气,乙生成丙,乙是水。
(1)甲分解成生成乙和丙的反应是过氧化氢二氧化锰催化作用下生成水和氧气,反应的化学方程式为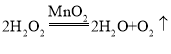 。
。
(2)甲是过氧化氢,由过氧化氢分子构成的,乙是水,由水分子构成的,从微观角度解释甲、乙性质有些差异的原因是构成分子不同。

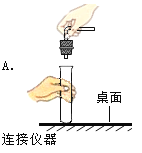
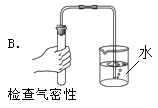
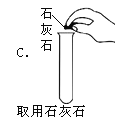
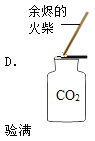
【题目】活动探究三:蜡烛燃烧的探究
甲乙两小组按下图所示实验探究蜡烛的燃烧产物,获得了不同的实验现象。
甲组:烧杯内壁有无色液滴
乙组:烧杯内壁有无色液滴,烧杯底部附着有黑色固体
【提出问题】同学们查阅教材实验,得知无色液滴是水(H2O),但黑色固体是什么呢?
【猜想】 小芳同学猜想黑色固体的主要成分是碳,小勇同学猜想是二氧化碳,你认为哪位同学猜想合理___________,理由是______________________________。
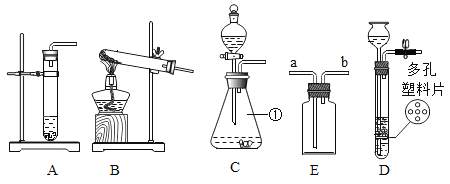
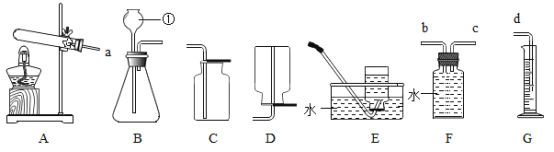
【实验验证】利用下图所示装置,甲、乙小组的同学分别设计了以下方案进行实验验证你的猜想。
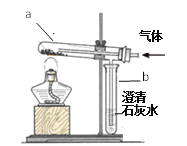
实验操作 | 实验现象 | |
甲组 | 取少量该黑色固体于a中,通入空气,点燃酒精灯加热。 | 黑色固体燃烧,不剧烈,发出_______光, b中溶液变浑浊。 |
乙组 | 取少量该黑色固体于a中,通入______,点燃酒精灯加热。 | 黑色固体剧烈燃烧,发出白光,b中溶液变浑浊。 |
【分析与结论】
(1)实验结束时,停止通入气体,后续两步操作的顺序应是_____
A. 先熄灭酒精灯,停止加热,再移走有澄清石灰水的试管
B..先移走澄清石灰水的试管,再熄灭酒精灯停止加热。
(2)b中的实验现象说明黑色固体燃烧生成了____________。
【反思】
(1)进一步实验发现,罩在火焰上方的烧杯位置越低,产生黑色固体越多。查阅资料可知:蜡烛+氧气(足量)→二氧化碳 + 水;蜡烛+氧气(少量)→ 一氧化碳 + 水;……
由此推测乙组实验产生黑色固体的原因是___________。
(2)甲、乙小组最终证明了蜡烛中一定含有_____(填字母序号)。
A. 碳、氢和氧三种元素 B. 碳和氧两种元素 C. 碳和氢两种元素
【题目】金属是现代生活和工业生产中应用极为普遍的一类材料。

(1)青少年看书、写字一定要爱护眼睛,台灯在光线不足时常用照明用具。图1中灯管后面的反光片为铝箔铝块能制成铝箔利用了铝的________性;
(2)Mg、Cu、Fe三种金属在稀盐酸里的反应现象如图2所示。图2中X所代表的金属是_______(填“Cu”或“Fe”);
(3)下列有关金属元素及其单质、化合物排列顺序正确的是___________;
AMn元素的化合价
B利用金属的年代:
C铜元素的质量分数
D元素的含量![]()
(4)金属的开发和利用是人类文明和社会进步的标志。美国普度大学研发出一种制备氢气的新工艺,流程如下图所示。

①此流程中,铝镓(Ga)合金________(填“可以”或“不可以”)循环使用;
②写出铝镓合金与水反应的化学方程式____________________。
(5)已知某金属粉末中除含有Al外还含有一定量的Fe和Cu,为证明Fe和Cu的存在并测定其中Al的质量分数,某化学兴趣小组的同学展开了如下的实验探究。
资料在线:Al与氢氧化钠溶液反应生成溶于水的偏铝酸钠和氢气(反应的化学方程式为:2Al+2H2O+2NaOH=2NaAlO2+3H2↑),Fe和Cu不与氢氧化钠溶液反应。
①请完成证明金属粉末中存在Fe和Cu的实验设计:
实验操作 | 实验现象 | 结论 |
I.取少量的金属粉末于试管中,加入足量的氢氧化钠溶液 | _______________________ | 仅除去铝 |
II.将试管静置,弃去上层清液,加入足量的_____________(填试剂名称)。 | __________________________________ | 证明含有铁 |
III.将试管静置,弃去上层清液,多次洗涤剩余固体 | 剩余固体呈紫红色 | 证明含有铜 |
②为探究该金属粉末中Al的质量分数,取20 g该金属粉末,把100 g氢氧化钠溶液平均分成5份依次加入,充分反应后,过滤出固体,将其洗涤、干燥、称量。实验过程中得到的部分数据与图象如下:

加NaOH溶液的次数 | 第一次 | 第二次 | 第三次 | … |
剩余固体的质量/g | 1 7.3 | n | 11.9 | … |
I以上数据可知,上表中n的值为___________;
II该金属粉末中Al的质量分数为___________%